 B .
B .  C .
C .  D .
D . 

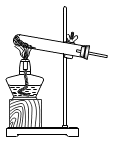 用甲装置制取氧气
B .
用甲装置制取氧气
B . 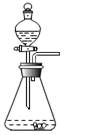 用乙装置制取二氧化碳
C .
用乙装置制取二氧化碳
C . 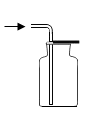 用丙装置收集氢气
D .
用丙装置收集氢气
D . 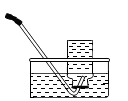 用丁装置收集氧气
用丁装置收集氧气


图示中属于单质的物质名称是,图示所表示反应的化学方程式为,该反应属于基本反应类型中的反应。
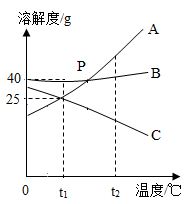
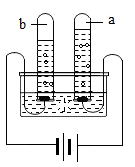

①吸收初期(通入废气体积小于V1),发生反应的化学方程式为;
②不断通入废气,最终产物是 。
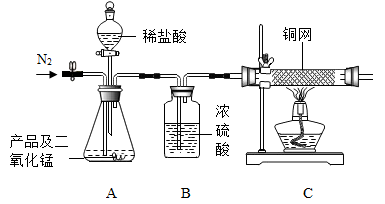
实验步骤:实验前称取产品及二氧化锰共12克,先缓慢通入氮气,一段时间后,加热铜网至红热,再缓慢滴入过量稀盐酸,直至A中样品完全反应。继续缓慢通入氮气,一段时间后停止加热,待C中铜网冷却后,停止通入氮气,将锥形瓶中的剩余物过滤,洗涤,干燥,得到滤渣2.0克。回答下列问题,
|
A组 |
B组 |
|
CH3COOK 36% KH₂PO4 14% CaCl2 14% MgCl2 36% |
CH3COOK 40% KH2PO4 14% CaCl2 15% KHCO3 31% |
回答下列问题