①原子由原子核和核外电子构成
②原子的质量主要集中在原子核上
③原子核在原子中所占的体积极小.
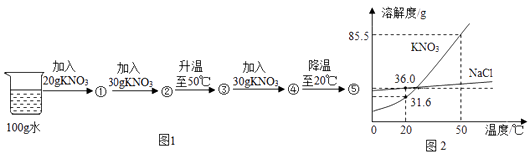
a.①、②均为不饱和溶液
b.②→③的过程中溶质质量分数变大
c.④→⑤的过程中析出KNO3晶体53.9g
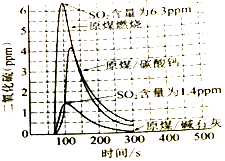
a.将原煤与碱石灰粉碎,混合均匀
b.将碱石灰的用量适当增加
c.将时间300s变为500s

①取14.06g还原铁粉在氧气流中充分加热,得到0.22gCO2;
②另取相同质量的还原铁粉与足量稀硫酸充分反应(FexC与稀硫酸不反应),得到0.48gH2 . FexC的化学式是.
【趣味实验】
实验1:和面.向20g面粉中加入10mL水,制得的面团编为1号;向20g面粉中加入10mL水,再加入2g膨松剂M,制得的面团编为2号.
实验2:发面.将和好的2个面团放入微波炉中加热,几分钟后,取出面团,发现1号面团无明显胀大,2号面团明显胀大且手感比较松软.
【提出问题】膨松剂M的成分是什么?
【提出假设】
假设1:M是NH4HCO3;
假设2:M是NaHCO3;
假设3:M是NH4HCO3和NaHCO3
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 取少量M于试管中,加热一段时间 | 无刺激性气味 试管内壁有水珠 试管内有固体剩余 | 假设成立 假设不成立 |
【实验探究2】
实验②:将实验①所得固体继续加热,无明显现象.冷却,向试管中加水,固体全部溶解,将所得溶液分为2份;向其中1份溶液中滴加稀盐酸,有气泡生成,将生成的气体通入澄清石灰水,有白色沉淀;向另1份溶液中滴加足量氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液不变红.
【得出结论】
实验①试管中剩余固体是(填化学式)
①NH4HCO3受热分解的化学方程式是.
②受热稳定性:Na2CO3(填“>”“=”或“<”)NaHCO3 .
某品牌复配膨松剂N的配料为:磷酸二氢钙、碳酸氢钠和玉米淀粉,N遇水会发生如下反应:Ca(H2PO4)2+2NaHCO3═CaHPO4↓+Na2HPO4+2CO2↑+2H2O;利用N和面和发面(加热)时,面团都会胀大.下列叙述正确的是(填序号)
a.常温下的溶解度:Na2HPO4>CaHPO4
b.碳酸氢钠在水溶液中遇到酸性物质能产生气体
c.根据上述反应,产生0.22gCO2至少需要NaHCO3的质量为0.42g.
SiO2 Si(粗)
SiHCl3
Si(纯)
步骤②经过冷凝得到的SiHCl3中含有少量的SiCl4和HCl,采用蒸馏来提纯SiHCl3 , 蒸馏属于(填“物理变化”或“化学变化”)

下列叙述正确的是(填序号)
a.石墨烯是单质 b.石墨烯是化合物 c.石墨烯不导电
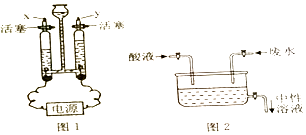
水和软水;自来水厂对天然水进行净化的过程中,通常不会采用(填序号)
a.电解 b.吸附 c.消毒