 沼气生产
B .
沼气生产
B .  石油蒸馏
C .
石油蒸馏
C .  转炉炼钢
D .
转炉炼钢
D .  高炉炼铁
高炉炼铁
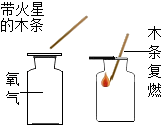 检验是否是O2
B .
检验是否是O2
B . 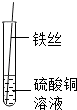 铁丝浸在硫酸铜溶液中
C .
铁丝浸在硫酸铜溶液中
C . 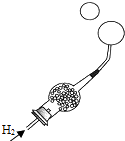 证明H2比空气轻
D .
证明H2比空气轻
D . 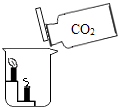 倾倒CO2
倾倒CO2


|
| IA | 0 | ||||||
| 1 | | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | | | | | | | | |
| 3 | | | | Z | | | | |
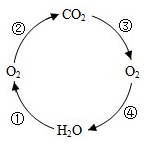
a.图中③是自然界中消耗二氧化碳的主要途径,其名称为。
b.写出图中①反应的化学方程式:。
C、丙均为黑色粉末,C和E在高温条件下可生成丙和D,其余反应条件、部分反应物和生成物均已略去。试推断:


①生成物只有氧气 ②不需加热 ③需加热
①控制液体的滴加速度 ②用体积较小的锥形瓶 ③加热反应物
实验时需将镁条进行打磨,其目的是。

(发现问题)
反应后甲同学用pH试纸测定试管中溶液的酸碱性,发现pH小于7,说明甲同学所得溶液呈性,(选填“酸”“碱”或“中”)。
(提出猜想)
甲同学:猜想Ⅰ:稀盐酸过量,使溶液pH小于7;猜想Ⅱ:氯化镁溶液pH小于7。
乙同学:猜想Ⅰ:氯化镁溶液使酚酞变红色;猜想Ⅱ:镁与热水反应使酚酞变红色。
(实验与思考)
为验证猜想,甲、乙两同学均需测定溶液的酸碱性,实验表明该溶液显弱酸性。乙同学为完成猜想Ⅱ,在滴有两滴酚酞的热水中放入一段打磨过的镁条,观察到溶液很快变为红色,同时还观察到镁条表面有气体生成,收集并点燃该气体,发现能燃烧,请根据实验现象写出镁与热水反应的化学反应方程式。
(结论)
镁与稀盐酸反应,镁反应完全后所得溶液显酸性;
镁与稀盐酸反应,镁过量时所得溶液显碱性。
|
甲 |
乙 |
丙 |
|
|
烧杯+稀硫酸 |
150g |
100g |
100g |
|
加入的铁样品 |
6g |
6g |
10g |
|
充分反应后,烧杯+剩余物 |
155.8g |
105.8g |
109.8g |