 B . 塑料瓶
B . 塑料瓶  C . 玻璃瓶
C . 玻璃瓶 
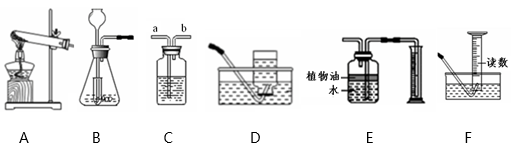
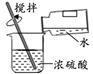 B . 取用液体
B . 取用液体 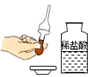 C . 测溶液pH
C . 测溶液pH 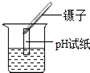 D . 读出液体的体积
D . 读出液体的体积 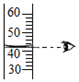

| 选项 | a | b |
| A | H2O | NH4NO3 |
| B | H2O | CaO |
| C | 稀H2SO4 | Zn |
| D | 稀HCl | NaHCO3 |
| 实验操作 | 现象 | 结论 | |
| A | 把燃着的木条插入某瓶无色气体中 | 木条熄灭 | 瓶中的气体是CO2 |
| B | 往久置于空气中的氢氧化钠溶液中滴加稀盐酸 | 有气泡产生 | 氢氧化钠溶液已变质 |
| C | 往某无色溶液中滴加氯化钡溶液 | 有白色沉淀生成 | 无色溶液中一定含有SO42- |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是CH4 |
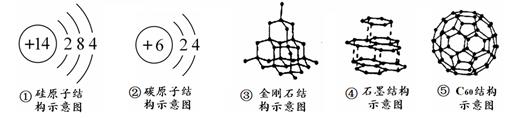
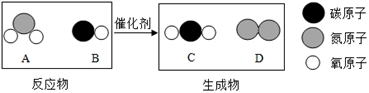
根据所学知识和上图所示的信息,回答问题:
硅元素化学性质与碳元素相似的原因是;
硅元素和氯元素组成的化合物的化学式为。
步骤I:取少量混合物加足量的水充分搅拌,有白色不溶物生成,过滤;
步骤II:在滤出的白色不溶物中,加入足量的盐酸,白色不溶物全部溶解;
步骤III:在步骤II所得的溶液中,加入硝酸银溶液,生成白色沉淀,再加入稀硝酸经振荡沉淀不溶解。
根据上述实验现象,回答问题:
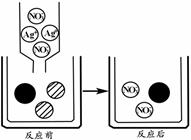
步骤Ⅰ:向3支大小相同的试管abc中加入相同体积(2mL)5%H2O2溶液;
步骤Ⅱ:向试管a中加入少量MnO2粉末,向试管b中滴加1~2滴10%FeCl3溶液。
得出实验结论:MnO2和FeCl3均能加快H2O2的分解速率,均作催化剂,且前者的催化效率高得多。
回答问题:
①步骤I中分别向3支试管中加入相同体积的溶液的目的是。
②设计试管c的作用是。
③若继续用上述实验药品研究温度对H2O2分解速率的影响,为了便于观察,你选择的催化剂和选择它的原因是。
实验仪器:试管、烧杯、量筒、天平、秒表;
实验药品:铝片、铝粉、5%盐酸、15%盐酸、冷/热水;
①利用所提供实验用品,研究的化学反应速率的影响因素是。
②请使用上面提供的实验用品,设计实验完成温度对化学反应速率的影响,说明实验步骤(文字表述、图示均可)。

查阅相关资料得知:
①辉铜矿主要含有硫化亚铜(Cu2S)、还有Fe2O3、SiO2及一些不溶性杂质。
②常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
回答问题:
A.CaO B.NaOH C.Cu D.Cu(OH)2
A 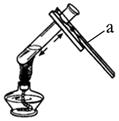 B
B 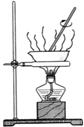
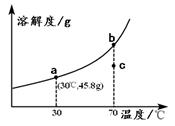
下表是氢氧化钙和氢氧化钠的溶解度数据
|
温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
|
溶解度 (g/100gH2O) |
氢氧化钙 |
0.19 |
0.17 |
0.14 |
0.12 |
0.09 |
0.08 |
|
氢氧化钠 |
31 |
90 |
111 |
129 |
313 |
336 |
|
请回答问题:
其理由是。
查阅资料,醋酸及其一些盐的相关性质如下:
|
物质 |
HAc |
NaAc |
Ca(Ac)2 |
Ba(Ac)2 |
Cu(Ac)2 |
|
在水中 的溶解性 |
溶于水,有剌激性气味 |
溶于水成无色溶液 |
溶于水成无色溶液 |
溶于水成无色溶液 |
溶于水成蓝色溶液 |
限选试剂是:醋酸溶液、BaCl2溶液、CaCO3粉末、稀盐酸、酚酞溶液、紫色石蕊溶液、镁条、碳粉、氧化铜粉末。
|
预测 |
预测的依据 |
验证预测的实验操作与预期现象 |
|
①能够与碳酸盐反应 |
|
取少量醋酸溶液于试管中,加入CaCO3粉末,振荡,若观察到,则预测成立。 |
|
②能够与 (填物质类别)反应 |
|
取少量醋酸溶液于试管中,,若观察到,则预测成立。 |
|
③能够与 (填物质类别)反应 |
|
取少量醋酸溶液于试管中,,若观察到,则预测成立。 |