 陶瓷花瓶
B .
陶瓷花瓶
B .  纯棉帽子
C .
纯棉帽子
C .  不锈钢水壶
D .
不锈钢水壶
D .  塑料油瓶
塑料油瓶

 稀释浓硫酸
B .
稀释浓硫酸
B .  量取液体体积
C .
量取液体体积
C .  闻气体的气味
D .
闻气体的气味
D .  滴加液体
滴加液体

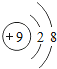 B .
B . 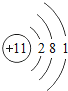 C .
C . 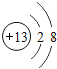 D .
D . 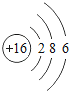

| 选项 | 实验目的 | 实验方案 |
| A | 除去CO2中的HCl气体 | 将混合气体通入足量NaOH溶液中 |
| B | 区分尿素CO(NH2)2、NH4Cl和NH4NO3 | 加熟石灰研磨闻气味 |
| C | 区分稀HCl、Na2CO3溶液、NaCl溶液 | 滴加紫色石蕊溶液观察颜色 |
| D | 除去KNO3溶液中的KCl | 加入过量的AgNO3溶液,过滤 |
①同种元素的微粒质子数一定相同,质子数相同的微粒不一定是同种元素
②中和反应一定生成盐和水,生成盐和水的反应也一定是中和反应
③同种分子构成的物质一定是纯净物,纯净物也一定由同种分子构成
④碱的溶液一定显碱性,显碱性的溶液不一定是碱的溶液
①一定质量的碳和氧化铜在密闭容器中充分反应 
②一定质量的二氧化锰和氯酸钾的混合物充分加热反应 
③等质量的金属镁、锌、铁分别放入足量的稀硫酸中充分反应 
④一定质量的氯化钡和盐酸的混合溶液中逐滴加入X溶液,X可以是碳酸钠或氢氧化钠 
①氮分子;
②三个硝酸根离子;
③氨气中氮元素的化合价;
④两个硫原子;
①NO2;
②Fe2+。
A食醋 B熟石灰 C石墨 D小苏打
①可用于厨房作调味品的酸是;
②可用于改良酸性土壤的碱是;
③可用于治疗胃酸过多症的是;
④可用于制铅笔芯的是;


①溶解度随温度升高而减小的是物质是;
②t3℃时将50g甲物质放到50g水中充分溶解后所得溶液的质量是g;
③某温度下,将丙的饱和溶液转化为不饱和溶液的方法之一是;
④将t3℃时甲、乙、丙三种物质的饱和溶液分别降温至t1℃,所得溶液中溶质质量分数由小到大的顺序。



(查阅资料)
①NaHCO3不仅可以与盐酸反应,也可以与NaOH溶液反应。与NaOH溶液反应的化学方程式为:NaHCO3+NaOH=Na2CO3+H2O。
②向NaOH溶液中通入少量CO2 , 反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O。继续通入过量CO2 , 反应的化学方程式为:Na2CO3+H2O+CO2=2NaHCO3。
(猜想与假设)猜想一:含有NaOH和Na2CO3;
猜想二:只含有;
猜想三:含有Na2CO3和NaHCO3;
猜想四:只含有NaHCO3。
(设计实验)
|
实验步骤 |
实验现象 |
解释或结论 |
|
①取少量样品于试管中,滴加几滴无色酚酞溶液 |
溶液呈红色 |
证明溶液显碱性 |
|
②另取少量样品于试管中,加入足量的BaCl2溶液,反应完全后,静置过滤 |
加入BaCl2溶液时观察到的现象是; |
证明溶液中有Na2CO3 |
|
③向实验②所得的滤液中滴加稀盐酸 |
有无色无味能使澄清石灰水变浑浊的气体产生 |
证明实验②溶液所得的滤液中有。 |
有同学认为实验①观察到的现象及结论足以证明溶液中有NaOH。你是否同意?请先回答再说出理由。