 B . “郫”字青铜戈
B . “郫”字青铜戈  C . 龙纹铅饼币
C . 龙纹铅饼币  D . 黄金面具
D . 黄金面具 





| 选项 | 问题 | 分析与设计 |
| A | 为何变质 | 2NaOH + CO2 = Na2CO3 + H2O |
| B | 是否变质 | 取样,加入足量稀盐酸,观察是否产生气泡 |
| C | 是否全部变质 | 取样,加入足量氯化钙溶液,观察产生沉淀多少 |
| D | 如何除去杂质 | 取样,加入适量氢氧化钙溶液,过滤 |
(提出问题)如何选择药品和设计装置进行测定?
(查阅资料)贝壳的主要成分是CaCO3 , 其它成分对实验影响忽略不计室温时,CaCO3不溶于水,CaSO4微溶于水
实验一:选择药品。分别取等质量颗粒状和粉末状的贝壳样品与等体积、等浓度的稀盐酸在图1的三颈烧瓶中反应,采集数据
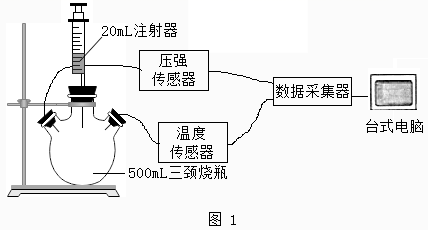
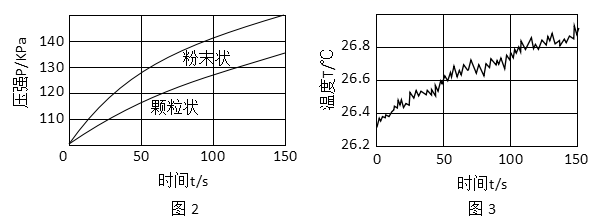
图1中反应的化学方程式是
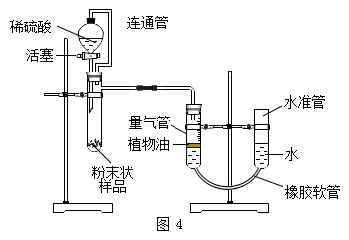
打开活塞,稀硫酸进入试管,观察到的现象是。反应结束后进行读数。读数前调节水准管与量气管液面相平的原因是

试剂a是
实验三中,样品质量为m g,加入稀硫酸体积为V1mL,加入氯化铵溶液体积为V2 mL,右侧针筒最后读数为V mL,则反应生成CO2体积为。该实验条件下CO2密度为d g/mL,则样品碳酸钙质量分数表达式为
与实验二相比,实验三的优点是(写一点)。