选项 | 事实 | 解释 |
A | 湿衣服在阳光下比在阴凉处干得快 | 温度越高,分子运动速率越快 |
B | 氧气和液氧都能支持燃烧 | 同种分子化学性质相同 |
C | 热胀冷缩 | 分子的大小随温度升降而改变 |
D | 水在通电条件下,可分解为氧气和氢气 | 化学反应中分子是可分的 |
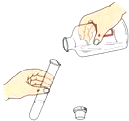 倾倒液体
B .
倾倒液体
B .  量取液体
C .
量取液体
C . 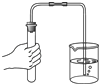 检查装置气密性
检查装置气密性


元素 | Na | Mg | ① | Si | P | ② | Cl |
原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
原子半径/10-10m | 1.86 | 1.60 | 1.43 | ③ | 1.10 | 1.02 | 0.994 |
最高正化合价 最低负化合价 | +1 | +2 | ④ | +4 -4 | +5 -3 | ⑤ | +7 -1 |
 B .
B . 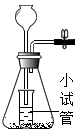 C .
C .  D .
D . 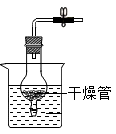

①则用“![]() ”可表示的微粒是 。(填化学式)
”可表示的微粒是 。(填化学式)
②同温同压下,气体的体积比等于其分子数目比。若空气中 1%的其它成分忽略不计,上图中可表示空气微观模型的是 (填字母)。
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳 0.2%的铁丝 | 含碳 0.6%的铁丝 |
燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧极少火星 | 剧烈燃烧少量火星 |
通过以上实验,说明铁丝燃烧时是否出现火星与 有关。
1加热熟石灰和氯化铵的固体混合物生成氨气。
2氨气是一种具有刺激性气味的无色气体,密度比空气小,极易溶于水。
3湿润的红色石蕊试纸遇到氨气变蓝色。
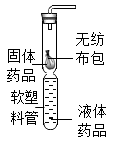
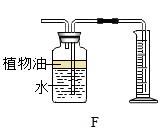
制取氨气的装置应与实验室用 (填“高锰酸钾”或“双氧水”) 制氧气的装置相同,氨气的化学式 。若用右图装置收集氨气,进气口应为 端(填“m”或“n”),检验氨气是否集满的方法是 。

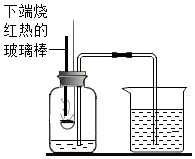
红磷燃烧的产物是 ;(填化学式)
a.加快集气瓶冷却
b.气管末端形成液封,防气体逸出
c.缓冲集气瓶内气压的骤然升高
【查阅资料】
1“暖宝宝”能耗尽容器中的氧气。
2“暖宝宝”的主要成分为铁粉、炭粉和少量氯化钠。
3“暖宝宝”发热的主要原理是铁粉与氧气、水共同作用生成氢氧化铁(铁的生锈)。
暖宝宝中少量氯化钠作用是 ;

重复 3 次上述实验及数据如下表。
试验次数 | 1 | 2 | 3 |
注射器剩余气体读数 | 18.7mL | 18.9mL | 18.8mL |
得出结论:根据表格中的实验数据计算,可知空气中氧气含量为 (用百分数表示)

实验中测得有关数据如下:
实验前 | 实验后 | |
浓硫酸的质量 | 301.3g | 304.9g |
NaOH 的质量 | 213.0g | 217.4g |
根据实验数据完成下列各题(写出每一步的计算过程):