



 收集H2
B .
收集H2
B .  O2验满
C .
O2验满
C .  配制20%的Ca(OH)2溶液
D . 除去CO中的CO2
配制20%的Ca(OH)2溶液
D . 除去CO中的CO2
选项 | 归类 | 物质(或元素) |
A | 常见碱 | 纯碱、烧碱、熟石灰 |
B | 常见合金 | 生铁、铜绿、硬铝 |
C | 常见干燥剂 | 浓硫酸、生石灰、碱石灰 |
D | 人体中常见微量元素 | 碘、锌、硒、钙等 |

![]()

![]()

序号 | 物质 | 选用试剂 | 操作 |
A | CO2(CO) | O2 | 点燃 |
B | Na OH溶液(Na2CO3) | 稀盐酸 | 加入试剂至不再产生气泡 |
C | KNO3溶液(KOH) | Cu(NO3)2溶液 | 加入适量的试剂,直接蒸发 |
D | FeSO4溶液(CuSO4) | H2O、Fe | 加水溶解、加入过量的Fe、过滤 |

 B . 向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量
B . 向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量 C . 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
C . 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应 D . 将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出
D . 将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出
A.熟石灰 B.一氧化碳 C.武德合金 D.硝酸铵 E.硫酸铜 F.肥皂水 G.氢氧化钠 H.纯碱

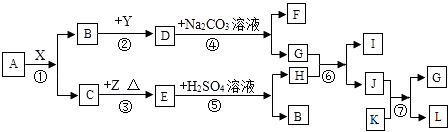

用C、F组合制取氢气的反应方程式为 。
若选用发生装置由B或C,为控制反应速率,你采取的措施可以是。
①G收集H2S,说明其密度比空气 (填“大”或“小”)。
② H装置的作用是:。

装置A的作用是。
设计的实验步骤为:
①精确称量样品,检查装置气密性;
②打开弹簧夹,鼓入空气,称量装置C;
③关闭弹簧夹,打开分液漏斗活塞;
④再打开弹簧夹,;
⑤再次称量装置C。
计算碳酸钠含量至少需要测定(填数字)个数据。根据制备反应,分析工业级NaN3中含有Na2CO3的可能原因。
精确称量0.140 g NaN3样品,设计如图装置,测定其纯度。已知2 NaN3 3N2 (NaN3中的N全部转化为N2 , 其他产物略),反应中放出大量的热。

检查该装置气密性的方法是连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做好标记,一段时间后,两边高度差(填“变大”、“变小”或“不变”),说明气密性良好。
