
 B . 读数偏小
B . 读数偏小  C . 污染待测液
C . 污染待测液  D . 液体飞溅
D . 液体飞溅 
颜色 | 红 | 橙 | 绿 | 蓝 | 紫 |
pH范围 | 1~3 | 4~5 | 6~7 | 8~10 | 11~14 |
 B .
B .  C .
C .  D .
D . 
| 选项 | 物质 | 杂质 | 试剂、方法 |
| A | 氮气 | 氧气 | 木条,点燃 |
| B | 稀硝酸 | 稀盐酸 | 加入适量的硝酸银溶液,过滤 |
| C | 氢氧化钠溶液 | 氢氧化钡溶液 | 加入适量的碳酸钠溶液,过滤 |
| D | 氧化铜 | 铜粉 | 空气中灼烧 |
| 序号 | 错误实例 | 错因分析 |
| A | 铁与稀硫酸反应生成硫酸铁 | 反应产物不正确 |
| B | FeCl3+3NaOH=Fe(OH)3+NaCl | 只缺少沉淀符号 |
| C | 2H2O=2H2↑+O2↑ | 反应条件不正确 |
| D | 氢氧化钠俗名烧碱或纯碱 | 俗名纯碱不正确 |
| 物质 | X | O2 | CO2 | H2O |
| 反应前的质量/g | 19 | 34 | 6 | 2 |
| 反应后的质量/g | 11 | 待测 | 28 | 20 |


① 金属表面除锈 ② 制造药物氯化锌 ③除去NaCl中的少量NaOH



①原子种类
②分子种类
③原子数目
④分子质量
⑤分子数目
⑥原子质量



①稀盐酸②酚酞溶液③二氧化碳④氯化钠溶液
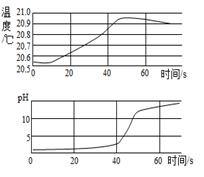
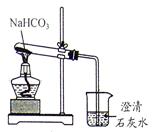
[提出问题]这瓶氢氧化钠固体是否变质?
[猜想假设]猜想一:没有变质,全部是NaOH;
猜想二:完全变质,全部是Na2CO3;
猜想三:。
[实验探究]为了探究固体成分,他们分别进行了如下实验:
⑴甲同学取少量固体于试管中,加水后有放热现象,说明这瓶固体中含有。
⑵写出氢氧化钠变质的化学方程式 。
⑶为了进一步确定这瓶固体的成分,丙同学设计了如下方案,请你完成下列实验报告:
|
实验步骤 |
可能观察到的现象 |
结论 |
|
Ⅰ、取样于试管中,加水溶解,滴入过量的(填化学式)溶液 |
产生白色沉淀 |
含有Na2CO3 |
|
Ⅱ、反应后过滤,取上层清液,滴人酚酞溶液 |
无色酚酞溶液变红 |
猜想正确 |
①SiO2+2C Si+2CO↑
②Si+2Cl2 SiCl4
③SiCl4+2H2 Si+4HCl




|
序号 |
第一次 |
第二次 |
第三次 |
第四次 |
|
加入稀盐酸的质量/g |
20 |
20 |
20 |
20 |
|
剩余固体的质量/g |
11 |
6 |
2.8 |
n |