
①实验Ⅰ中c处最先变黑;
②实验Ⅱ中若用干冷的烧杯,可以观察到烧杯内壁有水雾;
③实验Ⅱ中可能会观察到干燥烧杯内壁被熏黑;
④实验Ⅲ中,若用火柴点燃导管的另一端无火焰产生;
⑤实验Ⅳ中,蜡烛熄灭时产生的白烟是二氧化碳和水蒸气;
⑥实验Ⅳ中,蜡烛又被点燃是因为火柴直接将蜡烛点燃。

①温度升高 ②水分增多 ③氧气含量升高 ④二氧化碳含量升高


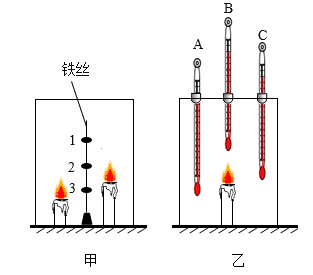
实验Ⅰ:如图甲,将三个盛有等量澄清石灰水的敞口容器编号,并等距离定在铁丝上,在铁丝两侧点燃高、低两支蜡烛,立即用玻璃罩扣上,使铁丝处于正中位置。三个容器内石灰水变浑浊所需的时间如表格所示。
| 容器编号 | 1 | 2 | 3 |
| 时间/秒 | 3.2 | 5.0 | 11.1 |
实验Ⅱ:如图乙,将三支温度计的玻璃泡分别置于玻璃罩内的不同位置。点燃蜡烛,一段时间后,观察到B的示数明显增大,A、C示数增大不明显。
A排队乘电梯依次撤离
B向着火楼层的上方撤离
C用湿毛巾捂住口鼻,弯腰跑离火场
D若火势不大,可用灭火器材将火扑灭

[查阅资料]
普通蜡烛由石蜡和烛芯制成,吹不灭的蜡烛在普通蜡烛的烛芯外包裹了一层打火石。打火石是在某种金属中掺入少量稀土元素制成的合金,它的着火点只有150℃蜡烛燃烧时包裹在石蜡内的打火石并不燃烧,当吹“灭”蜡烛时,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。
[问题与思考]
[实验探究]
吹不灭的蜡烛芯外的打火石含的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,他们决定继续探究。(不考虑打火石中稀土元素对探究金属性质的影响)
|
实验序号 |
实验操作 |
现象 |
结论 |
|
① |
取该打火石,用砂纸打磨后观察 |
打火石呈色 |
打火石中的金属一定不是铜 |
|
② |
取少量打磨后的打火石于试管中,加入稀盐酸 |
有气泡产生,溶液无色 |
打火石中的金属一定不是。 |
|
③ |
将少量打磨后打火石加入到硫酸铜溶液中 |
打火石表面有红色物质析出 |
打火石中的金属一定是镁 |
①实验3中涉及的化学方程式为。
②你认为实验3的方案是否合理(填“是”或“否”),如合理请说明理由,如不合理请设计一个方案进一步确认该金属是镁:。

|
操作 |
c处现象 |
d处现象 |
|
从a处缓缓吸气5次 |
无明显现象 |
石灰水不浑浊 |
|
从b处缓缓吹气5次 |
出现无色液滴 |
石灰水变浑浊 |
①吸气、吹气时,c处现象不同的原因是。
②吹气时,澄清石灰水变浑浊的化学方程式是。


①发出蓝色火焰;②燃烧后产生有刺激性气味;③发光、放热;④产生浓烟;⑤火焰分层