 B . 检查装置的气密性
B . 检查装置的气密性  C . 熄灭酒精灯
C . 熄灭酒精灯 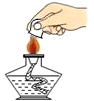 D . 加热液体
D . 加热液体 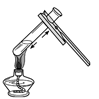
 B . 健康常识
B . 健康常识  C . 厨房中的化学
C . 厨房中的化学  D . 家庭小实验
D . 家庭小实验 
| 选项 | 问题和事实 | 解释 |
| A | 电解水生成氢气和氧气 | 水由氢分子和氧分子组成 |
| B | 施肥时氯化铵和熟石灰不能混合施用 | 氯化铵和熟石灰反应生成氨气,降低肥效 |
| C | 可用水润湿的 pH 试纸测雨水的酸碱度 | 雨水也会湿润 pH 试纸,故无影响 |
| D | 硫在氧气中燃烧时,集气瓶中先加少量水 | 以防止集气瓶炸裂 |


| 反应时间min/ 物质质量/g | 活性炭 | NO | 甲 | 乙 |
| 0 | 24.36 | 3 | 0 | 0 |
| 2 | 24 | 1.2 | x | 1.32 |
清洁剂名称 | 洁厕灵 | 84消毒液 |
有效成分 | HCl | NaClO |



材料一:合金是人类应用最早的金属材料.如青铜、黄铜(铜、锌合金,外观与黄金极其相似),合金比组成它的纯金属有更多优良性能,如抗腐蚀性好,硬度大等;
材料二:锂是银白色固体,质软,自然界密度最小的金属,跟水反应生成氢气和氢氧化锂。在电池,航空航天等领域有广泛的用途。
材料三:锂的原子结构示意图及他与钠在周期表中的信息如图所示。



|
药品/序号 |
A |
B |
C |
D |
|
金属 |
铜粉 |
锌粉 |
锌粉 |
镁粉 |
|
稀硫酸 |
9.8%硫酸 |
19.6%硫酸 |
9.8%硫酸 |
9.8%硫酸 |
①写出实验中一个反应的化学方程式。
②根据表中实验(选填序号),即可判断Mg、Cu、Zn三种金属的活动性顺序.
[提出问题]合金由哪两种金属组成?
[实验探究]①取该合金m1g,在足量氧气中反应,生成固体质量为m2g,m1和m2的关系如图所示,则(m2﹣m1)g表示的意义是。


|
实验次数 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
发光情况 |
明亮 |
亮 |
更明亮 |
较亮 |
较暗 |
微光 |
熄灭 |
熄灭 |
|
电压 U/V |
2.5 |
2.1 |
3.0 |
1.7 |
1.3 |
0.9 |
0.5 |
0.1 |
|
电流I/A |
0.28 |
0.26 |
0.30 |
0.24 |
0.21 |
0.19 |
0.16 |
0.05 |
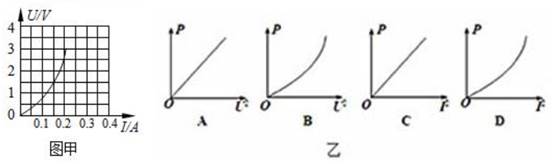
通过分析实验数据和计算可知:
① 灯泡的额定功率为W;通过小灯泡的电流与其两端电压不成正比,造成这种现象的原因是
②在第7、8两次实验中,灯泡熄灭的原因是
【查阅资料】①水溶液中的复分解反应一般朝着溶液中离子浓度(单位体积溶液中离子数目的多少)减少的方向进行.②了解到某些难溶性盐的溶解能力和颜色.
【实验取证】取一支试管,加入少量AgNO3溶液,再加入过量NaCl溶液,有白色沉淀生成.再往该试管中加入少量KI溶液,白色沉淀转化为黄色沉淀.
【分析讨论】
【得出结论】某些可溶性盐和难溶性盐之间能发生复分解反应.
【查阅资料】向碳酸钠溶液中逐滴加入稀盐酸的反应是分步反应,第一步反应生成碳酸氢钠和氯化钠,当碳酸钠反应完后才发生第二步反应。
丁同学向106g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为3.65%的稀盐酸,生成二氧化碳的质量变化如图2所示(不考虑CO2的溶解)。



测定某工业废气中SO2的含量,测试装置如图所示。
测试步骤:
①碘溶液的配制:准确称取1.27g碘单质,加入少量碘化钾,先溶解在100mL 水中,继续加水配制成1000mL 溶液。
②取5mL上述溶液,加入试管中,滴入2~3滴淀粉试液。
③把100mL注射器的活塞推到底后,插入试管的橡皮塞中,如图所示。

然后缓缓向外拉,使吸入试管内的废气与淀粉碘溶液充分接触。每次抽取的气体为100mL,重复抽取n次,直到溶液的颜色变为无色(废气中的其它成分不与淀粉碘溶液反应)。


实验步骤如下:
①按图连接装置并检查装置的气密性;
②取样品4.0g,置于甲中的硬质玻璃管内,乙中加入足量的氢氧化钠溶液;
③通入干燥的氧气一段时间后,电子秤的示数稳定在150.0g;
④继续保持氧气通入,点燃酒精喷灯,加强热;
⑤充分反应后(C被完全氧化,CaCO3被完全分解),最终电子秤的示数稳定在152.2g;
⑥实验结束后,根据实验所得的数据进行计算。
请回答下列问题: