
| 选项 | 有机物 | 鉴别所用试剂 | 现象与结论 |
| A | 苯酚与环己醇 | 碳酸氢钠 | 有气体放出的是苯酚 |
| B | 乙烯和甲醛 | 溴水 | 褪色的是乙烯 |
| C | 乙醛与甲酸甲酯 | 银氨溶液 | 能发生银镜反应的是乙醛 |
| D | 溴乙烷与煤油 | 氢氧化钠溶液 | 加热充分反应后,液体不分层的是溴乙烷 |
①淀粉、油脂在一定条件下都能发生水解反应
②淀粉和纤维素互为同分异构体
③食用油属于酯类,石蜡油属于烃类
④石油的分馏和煤的气化都是发生了化学变化
⑤淀粉遇碘变蓝色,在加热条件下葡萄糖能与新制Cu(OH)2悬浊液发生反应
①P4(白磷,s)+5O2(g)=2P2O5(s) ∆H1;
②4P(红磷,s)+5O2(g)=2P2O5(s) ∆H2;
③P4(白磷,s)=4P(红磷,s) ∆H3=-29.2 kJ·mol-1。
下列有关说法正确的是( )
| 选项 | 事实 | 结论 |
| A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间短 | 当其他条件不变时,升高温度,化学反应速率加快 |
| B | H+浓度相同的盐酸和醋酸分别与相同形状等质量的锌粒反应 | 反应开始时,速率相同 |
| C | 在容积可变的密闭容器中发生反应2NH3(g) | 正反应速率加快,逆反应速率减慢 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2--3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |


N2H4(g)+O2(g)=N2(g)+2H2O(g)△H1=﹣533.23kJ•mol﹣1
H2O(g)=H2O (l)△H2=﹣44kJ•mol﹣1
2H2O2(l)=2H2O(l)+O2(g)△H3=﹣196.4kJ•mol﹣1
则联氨与过氧化氢反应的热化学方程式可表示为( )


①HCHO(防腐剂) ② ![]() (车身亮光剂)③
(车身亮光剂)③ ![]() (香料原料)
(香料原料)
④ ![]() (杀虫剂原料)⑤CH3CH2CH2OH(有机溶剂)⑥CH3CHO(制塑料原料)
(杀虫剂原料)⑤CH3CH2CH2OH(有机溶剂)⑥CH3CHO(制塑料原料)

实验过程如上图所示,分析判断段化学反应速率最快(填OE、EF或FG)。

该反应的化学方程式:;

已知:①有机物B苯环上只有两种不同环境的氢原子;
②两个羟基连在同一碳上不稳定,易脱水形成羰基或醛基;
③RCHO+CH3CHO RCH=CHCHO+H2O;
④ 

①将9.2g该有机物完全燃烧,生成标况下15.68L的CO2和7.2g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
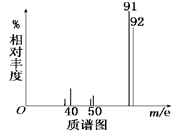

有关实验数据如 表:
| 相对分子质量 | 密度/(g·cm3) | 沸点℃ | 溶解性 | |
| 环已醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:在a中加入20 g环己醇,冷却搅动下慢慢加入1mL浓硫酸。c中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.当烧瓶中只剩下很少量的残渣并出现阵阵白雾时停止蒸馏。
分离提纯:将e中粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g。