 B . 道尔顿
B . 道尔顿  C . 门捷列夫
C . 门捷列夫  D . 拉瓦锡
D . 拉瓦锡 
 B .
B .  C .
C .  D .
D . 
 B . 检查气密性
B . 检查气密性  C . 点燃酒精灯
C . 点燃酒精灯  D . 取块状药品
D . 取块状药品 

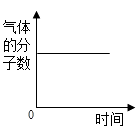 B .
B . 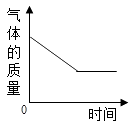 C .
C . 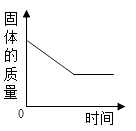 D .
D . 
食盐中添加有少量碘酸钾,可预防碘缺乏症。碘缺乏症中的“碘”是指(填“原子”“分子”或“元素”)。低钠盐中添加了一定量的氯化钾,适合中老年人和高血压患者长期食用。标出氯化钾中钾元素的化合价(用化学符号表示)。
工业上用石英(主要成分为SiO2)制备粗硅的反应的化学方程式为:SiO2+2C Si+2R↑,则R的化学式为,写出另一个有R生成的化学方程式 。

氨是一种重要的化学物质,可用于制造硝酸和氮肥。氨主要来自于人工合成。1909年,弗里茨·哈伯成功地利用氮气和氢气合成出氨。工业合成氨的流程如图(左)所示。为了找到合成氨反应合适的催化剂,人们做了6500多次实验,发现铁触媒效果较好。在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨,当容器中氨的含量不再发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如图(右)所示。1913年第一座合成氨工厂建立。如今全球合成氨年产量超千万吨,其中大约85%的氨用于生产氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
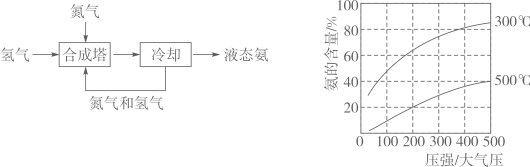
a、200大气压、300℃
b、200大气压、500℃
c、400大气压、300℃
d、400大气压、500℃


A 先检查装置的气密性,后加入药品 B 先固定试管,后放置酒精灯 C 先将导管伸入集气瓶,后加热试管


①红磷燃烧产生的明显现象是。
②反应的化学方程式为。
③该实验的原理:红磷燃烧消耗了空气中的氧气,瓶内的气压(填“增大”或“减小”),烧杯中的水倒吸进入瓶内,进入瓶内水的体积就是被消耗的氧气的体积。正常情况下,进入瓶内水的体积约占瓶内空气体积的。
(查阅资料)相同条件下,气体的压强与气体所占的体积成正比。
(设计与实验)
小组同学按图1装置进行实验,分别将红磷、硫放入集气瓶中燃烧,采集数据如图2、图3(注:装置气密性良好,P 0是瓶内初始气压,P1和P2是反应结束恢复到室温时瓶内的气压)。

(问题与现象分析)
燃烧匙内所装红磷或硫的多少对实验结果(填“有”或“无”)影响。
由图3压强关系P2 ≈ P0可知,(填“能”或“不能”)用硫代替红磷测定空气中氧气的含量。