 B . 过滤粗盐水中的泥沙
B . 过滤粗盐水中的泥沙  C . 量取48mL水
C . 量取48mL水  D . 倒入稀盐酸
D . 倒入稀盐酸 


 B . 地壳中元素含量
B . 地壳中元素含量  C . 空气组成
C . 空气组成  D . 原子结构
D . 原子结构 
软水是指不含或含较少可溶性钙、镁化合物的水。蒸馏水、自然水中的雨水和雪水属软水。硬水是指含有较多可溶性钙、镁化合物的水。
当硬水中的钙和镁主要以碳酸氢盐形式(Ca(HCO3)2、Mg(HCO3)2)存在时,这些盐在水被煮沸时便会发生分解,变成碱式碳酸盐沉淀析出而除去。因此,这种硬水称为暂时硬水。如果硬水中的钙和镁主要以硫酸盐、氯化物、硝酸盐的形式存在,当水煮沸时,这些盐不会沉淀,无法除去,这种硬水称为永久硬水。
A合理使用化肥可减少对水体的污染 B硬水和软水一定属于混合物
C煮沸不能降低永久硬水的硬度 D锅炉用水应当经过软化处理




向装有呼出气体的集气瓶中滴加少量澄清石灰水,振荡后观察到。
兴趣小组同学用图1所示装置进行实验。(锥形瓶内充满人体呼出的气体)实验前注射器内液体体积为50mL,向锥形瓶内注入少量液体后,注射器内的液体开始被自动吸入锥形瓶,完全反应后,注射器内NaOH溶液的体积为30mL。
结论:人体呼出气体中CO2的体积分数为。
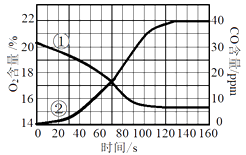
兴趣小组同学用图2所示装置进行实验。(注射器及玻璃管内充满人体呼出的气体)
1实验中需反复推拉注射器的目的是;
2在操作中如何判断装置中的O2是否反应完?。
结论:人体呼出气体中O2的体积分数为16%。
②小组同学准确测量人体呼吸前后气体的体积分数如下表所示:
|
氮气 |
氧气 |
二氧化碳 |
水 |
其他 |
|
|
呼入气体 |
78% |
21% |
0.03% |
0.06% |
0.91% |
|
呼出气体 |
75% |
15% |
3.68% |
5.44% |
0.88% |
你认为呼吸过程中,氮气含量减少的原因是。

他查阅资料得知:Fe2O3也可作KClO3;分解制O2反应中的催化剂。进行如下实验:
写出该反应的文字表达式;
他调节KClO3和Fe2O3的质量比制备O2 , 整理数据绘制出图2,从图中得出KClO3和Fe2O3最佳质量比是。
变化规律:;
分析原因:。