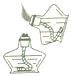
 点燃酒精灯
B .
点燃酒精灯
B .  闻气体气味
C .
闻气体气味
C . 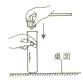 塞进橡皮塞
D .
塞进橡皮塞
D .  量筒读数
量筒读数
 B .
B .  C .
C .  D .
D . 

| A生活常识(灭火原理) | B 安全常识 |
| 炒菜时油锅着火--倒入蔬菜灭火---降低着火点 森林着火--开辟一条隔离带---隔离可燃物 | 煤气泄漏--先打开排气扇开关 进入人迹罕见的山洞--做灯火试验 |
| C物质的俗称与类别 | D环保知识 |
| Na2CO3—纯碱、盐 Hg— —水银、单质 | 白色污染--大气中白色粉尘含量超标 过度施用农药、化肥--水污染和土壤板结 |

 B . 测定空气中氧气含量,实验应将木炭改为红磷
B . 测定空气中氧气含量,实验应将木炭改为红磷  C . 测定溶液的pH,应用玻璃棒蘸取溶液滴在pH试纸上
C . 测定溶液的pH,应用玻璃棒蘸取溶液滴在pH试纸上  D . 验证质量守恒定律,该化学反应应在密闭容器中进行
D . 验证质量守恒定律,该化学反应应在密闭容器中进行 
| 选项 | 物质 | 选用试剂 | 操作方法 |
| A | CO2气体(CO) | 足量的氧气 | 点燃 |
| B | 铜粉(铁粉) | 足量的硝酸银溶液 | 充分反应后过滤 |
| C | MnO2(NaCl) | 蒸馏水 | 溶解、过滤、干燥 |
| D | NaOH 溶液(Na2CO3) | 石灰水 | 加入过量的澄清石灰水,过滤 |
|
|
|
|
A. 加热一定质量的高锰酸钾固体 | B. 向一定质量的氢氧化钠溶液中加入稀盐酸至过量 | C.浓硫酸长期露置在空气中 | D. 用两份等质量、等质量分数的过氧化氢溶液制取氧气 |
①绿皮车使用的煤为三大化石燃料之一,此外化石燃料还有石油和。
②在钢轨上喷涂防锈涂料,可防止钢轨生锈。该防锈方法的原理是。
土豆是继水稻、小麦、玉米之后的第四大粮食作物,含淀粉、蛋白质、维生素C等多种营养物质,是餐桌上的美味食材。

表1鲜土豆中主要营养物质的含量(每100g)
| 蛋白质/g | 脂肪/g | 淀粉/g | 钙/mg | 磷/mg | 维生素C/mg |
| 1.5-2.3 | 0.4-0.94 | 17.5-28.0 | 11-60 | 15-68 | 20-40 |
土豆切开后发生褐变,用水浸泡能防止褐变,但会引起营养物质流失。用土豆片进行实验,测得其食用品质、淀粉含量和维生素C含量随浸泡时间的变化如下:

土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒,就算是把变绿、发芽的部位削掉,也不宜食用。除食用外,土豆还可以作为原料广泛用于医药、化工、纺织、造纸等工业中。
依据文章内容回答下列问题。
A浸泡30min比10min脆性分值高
B浸泡10min,硬度、咬碎感均无明显变化
C随着浸泡时间的增加,粘结性、弹性分值均降低
A土豆是四大粮食作物之一B土豆中维生素C含量最高
C用水泡可防止土豆片褐变D土豆开发应用的前景广阔



| A氧气的制备与性质 | B二氧化碳的制备与性质 |
| ⑴实验室用高锰酸钾制取氧气,反应的化学方程式为。 ⑵E中的反应的方程式为。 | ⑴实验室制取二氧化碳,反应的化学方程式为。 ⑵F中旋紧瓶盖后振荡,瓶中发生反应的化学方程式为。 |

①a处只放白磷,b处只放红磷,Y型管中可以观察到的现象是。写出反应的化学方程式:。
②若要研究可燃物燃烧的另一个条件,在a处只放白磷,则应在b处加入。
①已知稀硫酸与碳酸钠的反应与实验室制取二氧化碳反应原理类似,稀硫酸与碳酸钠反应的化学方程式:。
②在装置Ⅱ的Y型管c、d处各放一张湿润的紫色石蕊滤纸条,将装置Ⅰ的Y型管向右倾斜,使少量稀硫酸流入碳酸钠中,观察到d处滤纸条先变红,该现象可说明。
③若要证明②中使紫色石蕊滤纸条变色的原因是H2O与CO2共同作用,而不只是CO2 , 则应在装置Ⅱ的Y型管内d、e处分别放置的实验用品是。
(猜想与假设)假设一:与反应初始温度有关;猜想二:与稀硫酸的浓度有关
用砂纸打磨镁条,进行下列实验。打磨的目的是。
|
|
反应初温/℃ |
镁的形状 |
稀硫酸的浓度/% |
气体的体积/mL |
|
① |
20 |
镁条 |
5 |
40 |
|
② |
20 |
镁条 |
10 |
55 |
|
③ |
30 |
镁条 |
10 |
62 |
写出镁与稀硫酸反应的化学方程式。
实验②和③比较,镁与稀硫酸反应快慢与有关。
实验①结束时测得溶液的温度为30℃,该反应属于(填“吸热”或“放热”)反应。