 C . 结构示意图为
C . 结构示意图为  的原子,可表示为
的原子,可表示为 | 选项 | 叙述I | 叙述Ⅱ |
| A | 硝基苯的沸点比苯的沸点高 | 硝基苯和苯可通过蒸馏初步分离 |
| B | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
| C | Na2S 还原性强 | Na2S用于除去废水中的Cu2+和Hg2+ |
| D | 酸性:HCl>H2S | 非金属性:Cl>S |
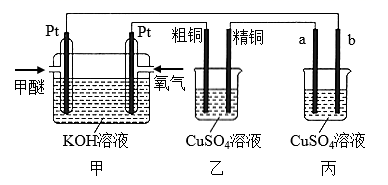

 )的说法正确的是( )
)的说法正确的是( )

 ),电解时
),电解时 


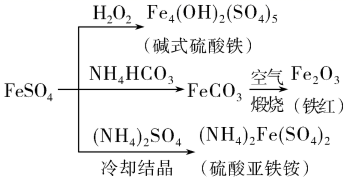
已知: ,该反应较缓慢,待生成一定量
时突显明显棕色。
实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是。
|
实验序号 |
温度(℃) |
6mol/L硝酸(mL) |
铜片(g) |
NaNO2(g) |
B中溶液变色的时间(s) |
|
① |
25 |
20 |
5 |
0 |
t1 |
|
② |
25 |
20 |
5 |
1.0 |
t2 |
已知NO2与 H2O反应生成 HNO2和另一种常见的强酸,写出其反应的化学方程式。
①乙烯的燃烧热△H1=a kJ·mol-1;②N2(g)+O2(g)= 2NO(g) △H 2=b kJ·mol-1 , 则乙烯和NO 反应的热化学方程式:C2H4(g)+6NO(g)=2CO2(g)+3N2(g)+ 2H2O(l)△H =kJ·mol-1(用字母a、b表示)。

①如果要将图中 C点对应的平衡状态改变为B点对应的平衡状态,则应采取的措施是(填字母)。
A.升高温度 B.降低温度 C. 用更好的催化剂 D. 移去 SO3
②若A点对应实验中,SO2(g)的起始浓度为c0 mol·L-1 , 经过t min 达到平衡状态,则该时段用 NO2表示的平均化学速率为v(NO2)=mol·L-1·min-1。

①。
②平衡时体系压强为p kPa,Kp为用分压表示的平衡常数(分压=总压×物质的量分数),则平衡常数Kp=(用含p的式子表示)。

已知:Ag2CrO4为砖红色固体; 。
请回答下列问题:

|
T/℃ |
5 |
10 |
15 |
25 |
30 |
|
钪的萃取率/% |
91.3 |
96 |
97.1 |
97.3 |
98.0 |
|
钛的萃取率/% |
0.94 |
0.95 |
2.10 |
3.01 |
4.20 |
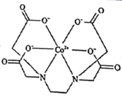 ,1mol 该配合物形成的配位键有mol,配位原子是,碳原子的杂化类型有。
,1mol 该配合物形成的配位键有mol,配位原子是,碳原子的杂化类型有。

 的合成路线(无机试剂任选)。
的合成路线(无机试剂任选)。