①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
 B .
B . 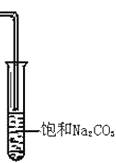 C .
C .  D .
D . 
| 选项 | 实验 | 现象 | 结论 |
| A | 某无色溶液, 加入足量的稀盐酸 | 生成无色无味的能使澄 清石灰水变浑浊的气体 | 说明原溶液中一定含有 CO |
| B | 将0.1mol/LMgSO4 溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 | 先有白色沉淀生成后变为浅蓝色沉淀 | Cu(OH)2的浓度积比 Mg(OH)2的小 |
| C | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3·H2O能大量共存 |
| D | 向稀硝酸中加入过量Fe粉,反应完全再向溶液中滴加 KSCN溶液 | 溶液变为血红色 | Fe与硝酸反应得到Fe3+ |


实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A,观察C中溶液颜色变化;
③将铜丝上提离开液面,停止加热。
雾霾中能形成酸雨的物质是。

①由图可知,1050K 前反应中 NO 的转化率随温度升高而堵大,原因是;1100k时,CO2的体积分数为。
②该反应达平衡后,为提高 NO 的转化率, 可采取的措施有(填字母序号)。
A.增大碳的质量
B.将 CO2 ( g )从体系中分离
C.降低温度
D.改用高效催化剂

石墨1 为 (填“正极” 或“负极”);正极的电极反应式为。

图1中化学键σ键与π键之比为;图2中碳原子的杂化方式为。

基态 Co 原子的价电子排布式为; 化合物 LiCoO2 中 O元素在晶胞中的位置,除了位于六棱柱的顶点外,其他具体位置是。

如表是部分金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 1.9 | 7.0 | 7.2 | 5.4 |
| 沉淀完全的pH | 3.2 | 9.0 | 9.5 | 8.2 |
请回答下列问题:
|
元素 |
Co |
Zn |
Cu |
Fe |
|
含量/% |
59.00 |
0.52 |
0.20 |
13.16 |
则煅烧后所得固体混合物中,钴氧化物的化学式是。
A.属于芳香族化合物,且只有1种官能团
B.能发生银镜反应
C.除苯环外不存在其他环状结构
其中核磁共振氢谐有4组峰的是(写出其中一种的结构简式)
 的合成路线
的合成路线