 点燃酒精灯
B .
点燃酒精灯
B .  量取5.5mL液体
C .
量取5.5mL液体
C .  过滤
D .
过滤
D .  稀释浓硫酸
稀释浓硫酸

| 选项 | 物质 | 杂质 | 试剂及操作方法 |
| A | KCl固体 | MnO2 | 加水溶解、过滤、洗涤、干燥 |
| B | FeSO4溶液 | CuSO4 | 加入适量的锌粉,过滤 |
| C | NaCl溶液 | FeCl3 | 加入过量NaOH溶液,过滤 |
| D | Cu | Fe | 加入过量的稀盐酸,过滤、洗涤、干燥 |
a.蛋白质 b.糖类 c.油脂 d.无机盐
a.KCl b.NH4NO3 c.KNO3 d.NH4H2PO4


a.t1℃时,用甲、乙、丙三种固体配制等质量的饱和溶液,所需水的质量大小关系是乙>甲>丙
b.t2℃时,甲、丙两物质饱和溶液中所含溶质质量相等
c.将t3℃时的甲、丙的饱和溶液降低温度至t2℃,所得溶液的溶质质量分数相等
d.乙中混有少量甲,可以采用蒸发结晶的方法提纯乙
①如果滤液呈无色,则滤渣中一定含有的金属是;
②如果滤液中加入稀盐酸有白色沉淀,则滤液中的金属阳离子有种;
③如果滤液呈浅绿色,则关于该滤渣和滤液的下列说法中正确的是。
a.向滤渣中加入稀盐酸,一定有气泡产生
b.向滤液中加入稀盐酸,一定有白色沉淀产生
c.滤渣中一定含有Ag
d.滤液中一定含有Fe(NO3)2 , 一定不含AgNO3 , 可能含有Zn(NO3)2

该同学对甲烷的其他化学性质产生了兴趣:
(查阅资料)无水硫酸铜遇水变成蓝色
(作出假设)甲烷具有还原性
(设计并进行实验)该同学按如图装置进行实验:

(实验现象与结论)
通入甲烷加热一段时间后才观察到A装置中黑色固体变为红色,B装置中无水硫酸铜变为蓝色,C装置中氢氧化钙溶液变浑浊。根据现象写出甲烷与氧化铜发生反应的化学方程式。通过实验证明,甲烷具有还原性。
实验时,先向装置中通入一段时间的氮气,再通入甲烷加热的目的是。
(提出问题)氢氧化钠是否变质?变质程度如何?
猜想I:没有变质,全部是NaOH;
猜想II:部分变质,固体是NaOH和Na2CO3;
猜想III:全部变质,全部是Na2CO3。
氢氧化钠变质的原因(用化学方程式表示)。
|
实验操作 |
实验现象 |
实验结论 |
|
|
小李 |
向第一份溶液中加入无色酚酞试液 |
溶液变红 |
猜想Ⅰ成立 |
|
小王 |
向第二份溶液中滴加几滴稀盐酸 |
无明显现象 |
猜想Ⅰ成立 |
|
小陈 |
向第三份溶液中加入CaCl2溶液 |
|
猜想Ⅲ成立 |
①小王和小陈认为碳酸钠溶液也能使无色酚酞试液变红,因此小李的结论不正确。
②经过讨论他们认为通过小王的实验不能得出样品中一定不含Na2CO3 , 原因是。
大家一致认为实验室的NaOH必须密封保存。
已知:①Na2CO3+CO2+H2O=2NaHCO3
②NaHCO3+NaOH=Na2CO3+H2O
如果向NaOH溶液中通入一定量的CO2气体,反应后所得溶液中溶质的组成有种情况(不考虑CO2和H2CO3作溶质)。
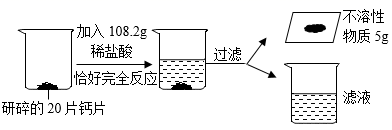
根据图示信息,完成下列各题: