 D .
D . 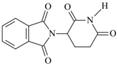 的说法不正确的是( )
的说法不正确的是( )
反应过程中的部分数据如下表所示:
| n/mol t/min | n(A) | n(B) | n(C) |
| 0 | 4.0 | 1.0 | 0 |
| 2 | 0.6 | 0.2 | |
| 4 | 0.4 | ||
| 6 | 2.8 | 0.3 |
下列说法正确的是( )


| | 滴定情况 |
| 10 | 溶液 |
| 20 | 溶液 |
| 20.11 | 恰好中和 |
|
实验 |
Ⅰ Ⅱ |
Ⅲ Ⅳ |
|
现象 |
无明显现象 |
Ⅲ中铝片表面产生细小气泡 Ⅳ中出现白色浑浊,产生大量气泡(经检验为 |
下列说法不正确的是( )
|
选项 |
实验操作和现象 |
结论 |
|
A |
向0.01 |
|
|
B |
室温下,向0.1 |
镁与盐酸反应放热 |
|
C |
向两支各装有5mL 0.1 |
草酸钠溶液浓度大的试管反应快 |
|
D |
向淀粉溶液中加适量20% |
淀粉未水解 |
|
序号 |
起始读数/mL |
终点读数/mL |
|
1 |
0.00 |
12.10 |
|
2 |
1.26 |
13.16 |
|
3 |
1.54 |
15.64 |
已知: ,
和有机物反应时也被还原为
。

|
化学键 |
C-H |
C-C |
| H-H |
| 键能/ | 412 | 348 | 612 | 436 |
请计算该反应的 。
a.高温 b.低温 c.高压 d.低压
①该反应的平衡常数表达式为 。
②掺入水蒸气能提高乙苯平衡转化率的理由是。
反应Ⅰ: ![]() ,
,
反应Ⅱ: ,
,
结合数据说明乙苯催化脱氢过程中加氧气的理由。
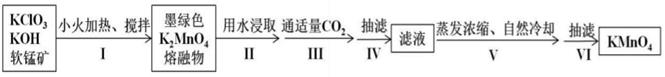
①在滴定操作前,需用移液管量取一定体积的草酸钠溶液于锥形瓶中。移液管放液的操作是,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管。
②滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→()→()→()→()→()→开始滴定。
A.烘干
B.装入滴定液至零刻度以上
C.调整滴定液液面至零刻度或零刻度以下
D.用洗耳球吹出润洗液
E.排除气泡
F.用滴定液润洗2至3次
G.记录起始读数
③滴定终点时,溶液颜色发生变化,未等半分钟即读数,结果读数后溶液又变回原色,则测得的高锰酸钾产品的纯度(填“偏高”或“偏低”或“不受影响”)。
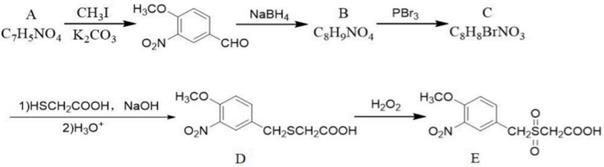
①存在 与苯环直接相连,且不存在
键。
②不同化学环境的氢原子数目比为1∶2∶6。
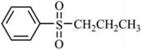 的合成路线流程图(无机试剂和有机溶剂任选,合成路线流程图示例见本题题干)。
的合成路线流程图(无机试剂和有机溶剂任选,合成路线流程图示例见本题题干)。