 B . 中子数为10的氧原子符号:
B . 中子数为10的氧原子符号:  B . 硅太阳能电池
B . 硅太阳能电池  C . 铅蓄电池
C . 铅蓄电池  D . 银锌纽扣电池
D . 银锌纽扣电池 
 B . 水煤气合成甲醇:
B . 水煤气合成甲醇: 
| 选项 | 事实 | 结论 |
| A | Na在空气中燃烧生成Na2O2 | Li在空气中燃烧生成Li2O2 |
| B | 浓硫酸可以干燥HCl气体 | 用浓硫酸干燥HI气体 |
| C | | |
| D | 硅是半导体材料 | 锗也是半导体材料 |

| 制取乙酸乙酯 | 比较乙酸和碳酸的酸性强弱 |
| | |
| 制取溴苯 | 石油分馏 |
| | |
①海水淡化的方法有(填一种)。
②下图是从海水中提取镁的简单流程:

工业上常用于沉淀Mg2+的试剂A的俗名是,Mg(OH)2转化为MgCl2的离子方程式是。


①无色无味液体 ②有毒 ③难溶于水 ④密度比水大
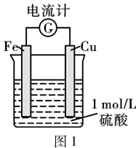
①该反应为(填“放热”或“吸热”)反应。
②下列措施中,能加快氢气生成速率的是(填字母)。
a.将铁片改成铁粉 b.将稀H2SO4改成浓硫酸 c.加硫酸钠溶液

①写出实验室用加热固体混合物的方法制备NH3的化学反应方程式。
②为比较不同催化剂的催化性能,需要测量并记录的数据是。
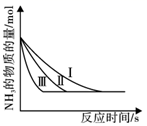
③在不同催化剂时测得混合气体中NH3的物质的量与时间的关系如图所示,则曲线(填序号)使用的催化剂催化性能最好,理由是。
|
元素 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径( |
0.74 |
1.60 |
0.53 |
1.10 |
0.99 |
0.89 |
0.75 |
1.43 |
|
最高或最低化合价 |
+2 |
+1 |
+5 |
+7 |
+2 |
+5 |
+3 |
|
|
-2 |
-3 |
-1 |
-3 |

| 实验操作及现象 | 实验结论 | |
| A | ①在漫射日光条件下,试管内:、液面上方有形成、内壁上出现了油状液滴 | ③CH4与Cl2在条件下发生化学反应 |
| B | ②迅速剥开黑纸,立即观察:试管内气体颜色为黄绿色 | |
④1 mol甲烷与足量Cl2发生取代反应时,得到最多的产物是(填化学式)。

①②装置中可盛放的试剂是:①、②(填字母)。
A. 品红 B. NaOH溶液 C. 溴水 D. 酸性高锰酸钾溶液
通过探究,该同学得出结论:甲烷和乙烯在不同条件下均能与卤素反应。