 B . 干燥氧气
B . 干燥氧气  C . 测定某溶液的 pH
C . 测定某溶液的 pH  D . 检查气密性
D . 检查气密性 
 B .
B .  C .
C .  D .
D . 

 B .
B .  C .
C .  D .
D . 




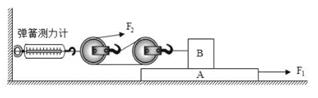
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | MnO2 | KCl | 加水溶解、过滤、蒸发 |
| B | NaCl | Na2CO3 | 加入足量稀硫酸,蒸发结晶 |
| C | CO2 | CO | 通过氢氧化钠溶液 |
| D | C | CuO | 加入足量稀硫酸,过滤、洗涤、干燥 |










|
额定电压 |
220V |
|
|
频率 |
50HZ |
|
|
额定功率 |
高温档 |
|
|
低温档 |
200W |
|

猜想一:Ca(OH)2溶液与CO2不反应,是CO2溶于水导致瓶内气压变小而变瘪。
猜想二:Ca(OH)2溶液与CO2反应,生成了可溶性物质
|
实验 |
步骤与操作 |
实验现象与结果 |
结论 |
|
一 |
1.取2个相同的软塑料瓶,分别集满CO2气体,编号为A、B。 |
两瓶内气体无色透明、瓶子形状正常。 |
Ca(OH)2溶液与 CO2发生了发生 了反应。 |
|
2.分别向A、B两瓶中加入等量的饱和Ca(OH)2溶液和 ? , 立即拧紧瓶盖并振荡。 |
两瓶内液体未出现浑浊;两瓶均变瘪,A瓶变瘪程度更大。 |
||
|
二 |
1.测山反应前Ca(OH)2溶液的pH。 |
大于7。 |
|
|
2.测出反应后 A 瓶内液体的 pH。 |
小于 7。 |

(查阅资料)草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2O CO2↑+CO↑+4H2O
碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。为了测定铁红中铁的质量分数,小组同学进行如下实验。(装置气密性良好,尾气处理装置未画出。)

①该实验为了保证进入 E 中的气体是纯净、干燥的 CO,则 B、C、D 中的试剂依次是(填字母序号)
a.浓硫酸b.澄清的石灰水c.氢氧化钠溶液
②对E装置加热后,要继续通入过量的CO,除了可以防止空气中的氧气再次将铁氧化,其它作用是:
③称取铁红样10.0g,用上述装置进行实验,测定铁红中铁的质量分数。若实验前后称得F装置增重8.8g,则此铁红中铁的质量分数是。
④如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会(选填“偏小”“不变”“偏大”)。





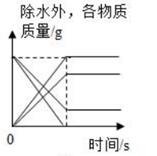
【方案一】用如图装置实验可计算出生成二氧化碳的质量。(常温常压下二氧化碳密度约为1.977 克/升)

若该大理石样品中碳酸钙的质量分数为 80%,则图中天平示数 m 的值为多少 g。
(写出计算过程)


| 额定电压/V | 220 |
| 额定运行功率/kW | 25 |
| 待机功率/kW | 1 |
| 最大载重/N | 4000 |
| 轿厢质量/kg | 500 |
为了安全,电梯设置了超载自动报警系统,其工作原理如图乙所示,控制电路的电源电压 U 为 12V,压力传感器的电阻 R 与所受压力 F 的关系图象如图丙所示,电磁继电器阻值可忽略。当控制电路中的电流大于 0.2A 时,会启动警报系统,同时无论如何按压电梯控制器,门电动机均不工作。