 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 取用液体药瓶
C . 取用液体药瓶  D . 称量氢氧化钠
D . 称量氢氧化钠 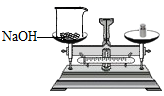
| | | | |
| 图1 | 图2 | 图3 | 图4 |

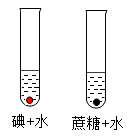 利用此实验比较不同物质在同种溶剂中的溶解性
B .
利用此实验比较不同物质在同种溶剂中的溶解性
B . 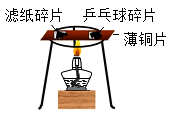 利用此实验探究可燃物燃烧所需的温度应达到着火点
C .
利用此实验探究可燃物燃烧所需的温度应达到着火点
C . 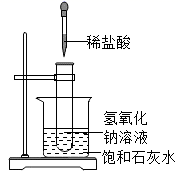 利用此实验验证稀盐酸和氢氧化钠溶液反应放热
D .
利用此实验验证稀盐酸和氢氧化钠溶液反应放热
D . 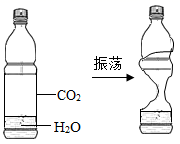 利用此实验证明二氧化碳能与水发生反应
利用此实验证明二氧化碳能与水发生反应
 向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
B .
向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
B .  恒温条件下,向盛有一定质量的硝酸钾饱和溶液的烧杯中加入硝酸钾固体
C .
恒温条件下,向盛有一定质量的硝酸钾饱和溶液的烧杯中加入硝酸钾固体
C . 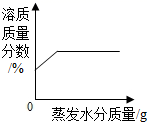 将一定质量的KNO3饱和溶液恒温蒸发水分
D .
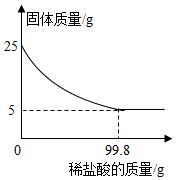
将一定质量的KNO3饱和溶液恒温蒸发水分
D .  向一定质量部分变质的NaOH溶液中滴加稀盐酸
向一定质量部分变质的NaOH溶液中滴加稀盐酸
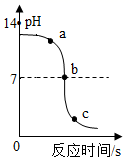
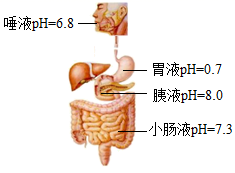
①图中碱性最强的体液是。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平[主要成分为Al(OH)3]治疗,其原理用化学方程式表示为 。
①疫情期间,某食品公司向医院捐赠了一批“即热米饭”,该“即热米饭”用生石灰和水的反应作为热源,请写出化学方程式。
②酒精与84消毒液[主要成分为次氯酸钠(NaClO)]不能混合使用。二者混合发生的一个反应的化学方程式是:C2H6O +7NaClO = 5X+ 2NaHCO3 + Cl2 ↑+ 2H2O,则X的化学式为。
①根据信息可知,维生素C溶液显(填“酸性”、“中性”或“碱性”)。
②在下列物质中,能与维生素C溶液发生反应的是(填选项序号)。
a 食盐 b 苛性钠 c 硫酸钠
③为较好吸收利用维生素C,食用黄瓜时宜(填“凉拌”或“煮熟”)。

信息:中和反应的微观实质是氢离子和氢氧根离子结合生成了水分子,即H+ + OH- = H2O。像这种用实际参加反应的离子符号来表示化学反应的式子叫离子方程式,离子反应遵守质量守恒定律。
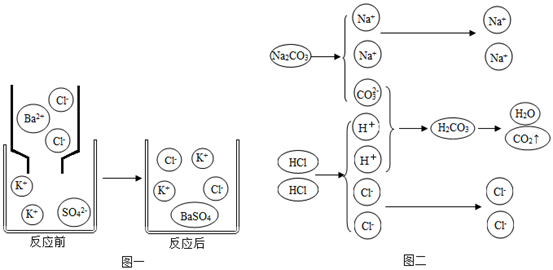
①采用过滤的方法除去泥沙等难溶性杂质,这是利用混合体系中各物质的不同从而将物质分离。
②为得到较纯的氯化钠,某同学向过滤后的盐水中加入下列三种药品:a Ba(OH)2溶液 b 盐酸c Na2CO3溶液。正确的加入顺序是(填字母)。加入Ba(OH)2溶液发生反应的化学方程式为。
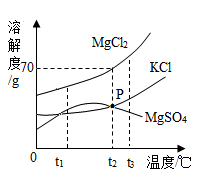
①选择苦卤更好理由是。
②工业生产中通常向苦卤中加入(写化学式)使其中的氯化镁转化为沉淀而分离出来。
如下图所示,同学们设计了不同的实验方案进行探究:
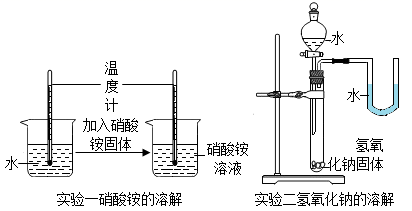
实验一中的硝酸铵溶解后,溶液温度(填“升高”、“降低”或“不变”)。
如下图所示,同学们用氢氧化钠溶液进行了下列实验,请分析并回答下列问题:
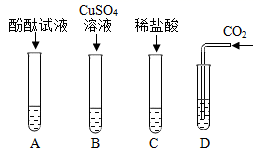
A试管中观察到的现象是 。
①为了证明D中已发生化学反应,某同学向该试管中再加入足量的 ,观察到有气泡产生。
②另一同学设计了如图所示实验方案,当观察到现象时,说明两者发生了化学反应。
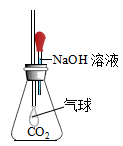
实验室中能用氢氧化钠溶液吸收的气体是(填字母)。
a 二氧化碳 b 水蒸气 c 氮气 d 氧气
(提出问题)猜想Ⅰ:没变质,全部是NaOH ;猜想Ⅱ:部分变质,既含有NaOH又含有Na2CO3;猜想Ⅲ:完全变质,全部是Na2CO3。
(查阅资料)i.已知信息: BaCl2 + Na2CO3 = 2NaCl + BaCO3↓
ⅱ.部分盐溶液在常温下的pH如下:NaCl =7 Na2CO3>7 BaCl2=7
|
实验步骤 |
实验现象 |
实验结论 |
|
步骤一:称取上述样品10.00g溶于50mL水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应,静置 |
|
久置固体中,一定含有 Na2CO3 |
|
步骤二:用干燥洁净的玻璃棒蘸取少量步骤一中充分反应后的上层清液滴在一小块pH试纸上,与比较,测出pH |
pH=11 |
久置固体中还一定含有(填化学式) |
滴加过量BaCl2溶液的目的是。