 B . 添加酒精
B . 添加酒精  C . 量取液体
C . 量取液体  D . 装药品
D . 装药品 


 B .
B .  C .
C .  D .
D . 
①84消毒液不能与洁厕灵混用,因为两者混合会发生如下反应:NaClO+2HCl=NaCl+X↑+H2O,其中X是一种有毒气体,它的化学式为。
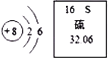
②NaClO中氯元素的化合价为。
③H2O属于(填序号)。
A.混合物 B.化合物 C.氧化物
①食盐是厨房重要的调味品,其主要成分氯化钠由(选填“分子”“原子”或“离子”)构成。
②宅家制作可乐鸡翅时当我们打开汽水瓶盖,有气泡冒出,说明气体溶解度随压强减小而。
③注意用火安全,若炒菜时油锅不慎着火,可以采取的灭火方法是。
④洗洁精除掉餐具上的油污,利用了洗洁精的作用。
⑤为节约水资源,生活中可以采取的做法是。
⑥菜刀洗后擦干,放在干燥处可以防止菜刀生锈,此法应用的防锈原理是。


②乙为通过红磷燃烧前后质量的测定验证质量守恒定律的实验。用红热的玻璃管引燃红磷,实验现象是:红磷燃烧,产生,放出大量热。实验中气球的作用除了使装置密闭之外,还可以防止实验时若取用红磷的量不足,对实验的结果(选填“有”或“没有”)影响。

试管a中的气体是,试管a和试管b中的气体体积比是,此实验的结论是,得出这种结论的依据是,电解水的化学方程式为。




(收集资料)绿色锈迹是铜长期暴露在空气中与氧气、水蒸气、二氧化碳等物质发生反应生成的碱式碳酸铜,俗称铜绿。
(分析推理)聪聪根据铜绿的形成过程认为铜绿中含有Cu、H、O、C等元素,他做出此判断的依据是。

观察到出现,说明铜绿中含有氢元素和氧元素。
(实验2)同学们想到要除去铁制品表面的铁锈可以将铁制品在酸溶液中浸泡一段时间,于是认为除去铜绿也可以使用酸溶液。小明取少量铜绿放置在试管中,加入适量稀盐酸,观察到粉末逐渐溶解,,溶液呈蓝色,说明用稀盐酸可以除去铜绿,并进一步证明铜绿的生成有二氧化碳参与。
实验1中,加热铜绿前先通入一会儿氮气的目的是。
