 倾倒液体
B .
倾倒液体
B .  过滤
C .
过滤
C .  检查气密性
D .
检查气密性
D .  检验氧气是否收集满
检验氧气是否收集满
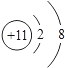 B .
B . 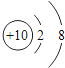 C .
C . 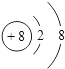 D .
D . 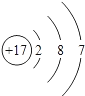


A 2H:“2”表示2个氢分子
B Mg2+:“2”表示镁元素的化合价为+2
C CO2:“2”表示1个CO2分子中含有2个氧原子
D Fe2+:“2”表示
|
选项 |
实验目的 |
实验方法 |
|
A |
鉴别KMnO4、KClO3、 P2O5三种固体 |
观察颜色 |
|
B |
分离糖和食盐 |
溶解、过滤 |
|
C |
鉴别水和浓氨水 |
滴入酚酞溶液 |
|
D |
鉴别软水和硬水 |
|

A 图中微量元素属于金属元素的有3种
B 锌原子核外电子数为30
C 硒原子在化学反应中容易得到2个电子形成阳离子



a、反应中氧气的物理性质发生了变化
b、此时得到的气体一定是混合物
c、若只加热氯酸钾,生成的气体无气味,说明刺激性气味一定与二氧化锰有关
d、可能是生成的氧气与残留在发生装置中的空气在加热的条件下反应生成了新物质
(提出问题)二氧化锰常作为氯酸钾分解制取氧气的催化剂,那其他氧化物是否也能催化氯酸钾分解呢?是否比二氧化锰催化效果更好?
(查阅资料)研究表明,许多金属氧化物对氯酸钾的分解(分解时放出热量)有催化作用,分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
|
氧化铁 |
氧化铝 |
氧化铜 |
氧化镁 |
|
|
开始反应 |
420 |
515 |
305 |
490 |
|
剧烈反应 |
490 |
540 |
350 |
545 |
Ⅰ、将3.0g氯酸钾放在试管中加热;
Ⅱ、将3.0g氯酸钾与1.0g二氧化锰混合均匀加热;
Ⅲ、将Xg氯酸钾与1.0g氧化铜混合均匀加热;
(实验现象分析)将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,称量得到1.0g黑色粉末,产生的现象与实验Ⅱ相同。
①实验Ⅰ和Ⅲ比较可证明。
②探究实验Ⅱ、Ⅲ,你认为Ⅲ中X的值应为。
①实验Ⅱ和Ⅲ对比的目的是。
②在相同温度下比较两组实验产生氧气的快慢,通常可采用的方法有:
①测量。
②测量。