纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 氯水 | 水煤气 | NaCl | 酒精 |
B | 氢氧化钡 | 冰水混合物 | 冰醋酸 | 硫酸钡 |
C | 胆矾 | 石灰水 | KOH | 二氧化碳 |
D | 硫酸 | 碳素钢 | 盐酸 | 氮气 |
 B . 渗析
B . 渗析 C . 萃取
C . 萃取 D . 丁达尔效应
D . 丁达尔效应

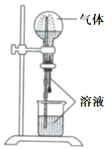
|
气体 |
溶液 |
|
|
A. |
H2S |
稀盐酸 |
|
B. |
HCl |
稀氨水 |
|
C. |
NO |
稀H2SO4 |
|
D. |
CO2 |
饱和NaHCO3溶液 |
选项 | 事实 | 原因 |
A | H2SO4是酸 | H2SO4中含有氢元素 |
B | 浓硝酸在光照下颜色变黄 | 浓硝酸具有挥发性 |
C | 在蔗糖中加入浓硫酸后出现发黑现象 | 浓硫酸具有吸水性 |
D | 用可溶性铝盐和氨水制备氢氧化铝 | 氢氧化铝碱性比氨水弱且很难与氨水反应 |
选项 | 物质 | 杂质 | 除杂质所用试剂和方法 |
A | NaHCO3固体 | Na2CO3 | 加热 |
B | KNO3 | K2SO4 | BaCl2溶液过滤 |
C | Cu | CuO | 稀硫酸,过滤 |
D | CaCO3 | CaO | 盐酸,过滤 |
①2MoS2+7O22MoO3+4SO2
②MnO3+2NH3·H2O=(NH4)2MoO4+H2O
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl
④H2MoO4MoO3+H2O
⑤用还原剂将MoO3还原成金属钼。则下列说法中错误的是( )
①稀硫酸 ②小苏打 ③水玻璃 ④二氧化碳 ⑤Na ⑥NaOH溶液 ⑦Na2O2 ⑧Al

①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为。
②酸浸时,通入O2的目的是。
③“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+ , 再用酸性K2Cr2O7 , 标准溶液测定Fe2+的量(Cr2O被还原为Cr3+),则SnCl2、Fe2+和Cr3+三者中还原性最强的是。

已知:NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO3+NaNO2+H2O
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋

回答下列问题:
84消毒液 有效成分:NaClO 规格:100mL 质量分数:25% 密度:1.19g/cm3 |