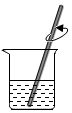
 溶解时,搅拌加速溶解
B .
溶解时,搅拌加速溶解
B .  稀释时,加速热量散失
C .
稀释时,加速热量散失
C .  蒸发时,转移固体
D .
蒸发时,转移固体
D .  测酸碱度时,取用少量液体药品
测酸碱度时,取用少量液体药品

| 选项 | 甲 | 乙 | 丙 |
| A. | 浓氨水 | —— | 无色酚酞溶液 |
| B. | 石灰水 | 碳酸钠 | 无色酚酞溶液 |
| C. | 稀盐酸 | 石灰石 | 紫色石蕊溶液 |
| D. | 浓盐酸 | 锌粒 | 紫色石蕊溶液 |
| 溶剂 | 氢氧化钠 | 碳酸钠 | ||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109g | 129g | 21.8g | 49g |
| 酒精 | 17.3g | 40g | 难溶 | 难溶 |

| 选项 | 问题 | 分析与设计 |
| A | 为何变质 | 2NaOH + CO2 = Na2CO3 + H2O |
| B | 是否变质 | 取样,加入足量稀盐酸,观察是否产生气泡 |
| C | 是否全部变质 | 取样,加入足量氯化钙溶液,观察产生沉淀多少 |
| D | 如何除去杂质 | 取样,加入适量氢氧化钙溶液,过滤 |

 A图:加水稀释NaOH溶液
B .
A图:加水稀释NaOH溶液
B .  B图:浓硫酸长时间敞口露置于空气中
C .
B图:浓硫酸长时间敞口露置于空气中
C .  C图:向饱和石灰水中加入CaO
D .
C图:向饱和石灰水中加入CaO
D .  D图:向稀硫酸和硫酸铜的混合溶液中加入KOH溶液
D图:向稀硫酸和硫酸铜的混合溶液中加入KOH溶液

|
序号 |
温度 |
水质量 |
加入NaCl质量 |
溶液质量 |
|
① |
20℃ |
25g |
9g |
34g |
|
② |
20℃ |
50g |
20g |
68g |
|
③ |
20℃ |
100g |
34g |
134g |
|
④ |
20℃ |
150g |
54g |
204g |
上述实验中,所得溶液为饱和溶液的是(填数字序号)。
①叠氮酸在水溶液中解离出H+和(填化学符号)。
②叠氮酸与NaOH溶液的反应属于(填基本反应类型)。
③叠氮化钠受热分解时产生两种单质,该反应的化学方程式为。

①盐酸可用于金属表面除锈,请写出盐酸除铁锈的化学方程式。
②利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图。当滴入溶液为V2mL时,形成溶液中所含溶质化学式为,所得溶液能使紫色石蕊溶液变成色。

①信息中提供的膨松剂是(填化学式);
②信息中的膨松剂能使蒸制或烘焙的食品疏松多孔,原理是(用化学方程式解释)。



①操作a的名称是。
②实验I中加入的试剂B是。(填序号)
a、稀盐酸b、碳酸钠溶液c、氢氧化钡溶液
③实验Ⅱ中发生中和反应的化学方程式是。

①为了使海水中含量较低的氯化镁富集,工业生产中通常向海水中加入物质A是(写化学式)使海水中的氯化镁转化为沉淀,该反应的化学方程式是,此过程富集氯化镁的同时也达到了的目的。
②反应Ⅲ的基本反应类型为。

上图中操作有错误的是(填数字序号,下同)。正确的实验步骤是。

指出图中称量步骤的不正确操作:;。

实验①的反应的化学方程式是,实验②的反应现象是,实验④反应的化学方程式是。
A.酚酞溶液 B.氯化钡溶液 C.硫酸铜溶液 D.硫酸钠
小组同学将④、⑤两支试管反应后的物质倒入同一洁净的烧杯中,充分反应后过滤,得到无色滤液和白色沉淀。同学们对白色沉淀的成分产生了兴趣,继续进行实验。
(作出猜想)
猜想一:;
猜想二:BaSO4、BaCO3。
(实验与结论)
完成表格
|
实验操作 |
实验现象 |
实验结论 |
|
取少量白色沉淀于试管中,向其中加入足量的稀盐酸 |
|
猜想二成立 |
演示实验中有一组不能用来验证酸的通性,该组是(填序号)。

(提出问题)生石灰样品的成分是什么?
(作出猜想)生石灰样品的成分可能是CaO、Ca(OH)2和CaCO3中的一种或几种。
|
实验 |
实验操作 |
实验现象 |
实验结论 |
|
① |
取样品于烧杯中,加水溶解,用手触摸烧杯壁。 |
烧杯壁发热 |
|
|
② |
取少量实验①烧杯中的物质过滤,向其中滴入。 |
溶液变红 |
有Ca(OH)2 |
|
③ |
另取少量实验①烧杯中的物质,向其中滴加少量稀盐酸。 |
|
无CaCO3 |
同学们经过讨论,发现通过实验②不能得出样品中一定含有Ca(OH)2 , 理由是。

(讨论与分析)该生石灰样品的成分是。
|
实验序号 |
1 |
2 |
3 |
4 |
5 |
|
加入CaCl2溶液质量/g |
15 |
15 |
15 |
15 |
15 |
|
生成沉淀的总质量/g |
3 |
| 9 | 10 | 10 |
求:
