 B . 粉碎矿石
B . 粉碎矿石  C . 淘洗矿粉
C . 淘洗矿粉  D . 取泥制坯
D . 取泥制坯 
 B . 点燃酒精灯
B . 点燃酒精灯 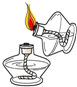 C . 加热液体
C . 加热液体 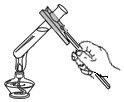 D . 倾倒液体
D . 倾倒液体 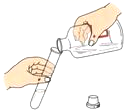





| 物质 | a | b | c | d |
| 反应前的质量/g | 40 | 5 | 16 | 15 |
| 反应后的质量/g | X | 5 | 30 | 26 |
一氧化氮(NO)是一种无色气体,熔点−163.6℃,沸点−151℃,密度比空气略大,不易溶于水。NO不稳定,易与空气中氧气发生反应,生成红棕色有刺激性气味的二氧化氮(NO2)。汽车尾气(含有CO与NO等物质)是城市空气的污染源,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO与NO反应,生成两种气体,一种是空气中体积分数最多的气体,另一种是光合作用的原料。NO被发现广泛分布于生物体内各组织中。1992年被美国Science 杂志评选为“明星分子”。NO在心脑血管调节等方面有着十分重要的生物学作用,是心脑血管的保护神。
依据文章内容,回答下列问题:
A 密度略大于空气 B 不易溶于水 C 易与空气反应

用高锰酸钾制取氧气。
①该反应的化学方程式为。
②从图1中选择组装发生装置所需的仪器(填字母)。
③仪器E的名称为。
用如图3装置测定“富氧空气”中氧气的体积分数(集气瓶容积为250mL,底部已加入20mL水)。烧杯中盛有V1mL的水,红磷充分燃烧后熄灭,冷却至室温后,打开止水夹,待右侧烧杯内液面不再变化,两边液面恰好相平,测出烧杯内水的体积为V2mL本次实验测得“富氧空气”中氧气的体积分数为(用含V1、V2的式子表示)。
猜想(1):该溶液中有过氧化氢的剩余。
猜想(2):该溶液中没有过氧化氢的剩余。
(方案讨论)为了验证猜想,甲、乙、丙三同学分别提出如下方案:
甲:取适量试剂于试管中,伸入带火星的木条,若带火星的木条复燃,则猜想(1)成立,若带火星的木条不复燃,猜想(2)成立。同学们认为此方案不行,原因是。
乙:取少量二氧化锰于试管中,加入与甲等量的试剂,若有气泡产生,则猜想(1)成立,若无气泡产生则猜想(2)成立,理由是(写化学反应的符号表达式)
丙:
|
操作 |
现象 |
结论 |
|
取与甲等量试剂于试管中,加热,伸入带火星的木条 |
|
猜想(1)成立 |
(得出结论)根据乙同学加二氧化锰后有气泡产生,以及丙同学的实验结论,得出最终结论:该溶液中有过氧化氢的剩余。
课外兴趣小组的同学利用如图装置测定该瓶过氧化氢完全分解生成氧气的体积,在实验过程中多多同学待有均匀连续气泡开始收集氧气,最终测定氧气体积会(填“偏大”“偏小”、“不变”),在实验过程中柚柚同学仰视读数,最终测定氧气体积会(填“偏大”、“偏小”、“不变”)。

实验操作:取30粒含MnO2的海藻酸钠微球,采用图1装置进行实验。改用另一种微球,分别重复上述实验,得到图2的锥形瓶内压强随时间变化的曲线图。

①每次实验时,海藻酸钠微球数应相同的原因是。
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是。
③从实验曲线看,催化效果较好、反应温和的催化剂是。