A | B | C | D |
|
|
|
|
速滑冰刀中的钛合金 | “飞扬”火炬中的聚硅氮烷树脂 | 颁奖礼服中的石墨烯发热材料 | 可降解餐具中的聚乳酸材料 |
A | B | C | D | |
实验 |
|
|
| 铜丝加热后,伸入无水乙醇中 |
现象 | 产生白色沉淀,最终变为红褐色 | 产生淡黄色沉淀 | 沉淀由白色逐渐变为黄色 | 先变黑,后重新变为红色 |

催化剂 | 金属元素的电负性 | 肉桂醛转化率/% | 苯甲醛选择性/% |
0.9 | 80.79 | 71.93 | |
1.0 | 78.27 | 60.51 | |
1.5 | 74.21 | 54.83 | |
1.6 | 76.46 | 48.57 | |
1.9 | 75.34 | 41.71 |
已知:i.选择性
ii.与
同主族。
下列说法不正确的是( )

已知:的性质与C相似,L可由
, 在酸催化下水解、聚合制得。下列关于硅橡胶的说法不正确的是( )
选项 | 实验操作 | 现象 | 解释或结论 |
A | 向某补血口服液中滴加几滴酸性 | 酸性 | 该补血口服液中一定含有 |
B | 用蒸馏水溶解 | 溶液由绿色逐渐变为蓝色 |
|
C | 将25℃ | 溶液的pH逐渐减小 | 温度升高, |
D | 将铜与浓硫酸反应产生的气体通入 | 产生白色沉淀 | 该气体中一定含有 |
①称取m g样品,配制成100mL溶液;
②取出25mL溶液置于锥形瓶中,加入2滴酚酞溶液,用浓度为的盐酸滴定至溶液恰好褪色(溶质为
和
),消耗盐酸体积为
;
③滴入2滴甲基橙溶液,继续滴定至终点,消耗盐酸体积为。
下列说法正确的是( )
投料比
温度/℃ | |||
200 | 1.70 | 0.21 | 0.02 |
250 | 2.73 | 0.30 | 0.06 |
300 | 6.00 | 0.84 | 0.43 |
350 | 7.85 | 1.52 | 0.80 |
下列说法不正确的是( )
序号 | ① | ② | ③ |
实验装置及操作 |
|
|
|
实验现象 | 溶液无明显变化 | 溶液立即变为黄色,产生大量无色气体;溶液温度升高;最终溶液仍为黄色 | 溶液立即交为棕黄色,产生少量无色气体;溶液颜色逐渐加深,温度无明显变化;最终有紫黑色沉淀析出溶液无明显变化 |
下列说法不正确的是( )

①硅原子的杂化方式为。
②已知晶胞的棱长均为a pm,则
晶体的密度
(列出计算式)。
资料:原硅酸( )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
①原硅酸钠溶液吸收空气中的
会生成
, 结合元素周期律解释原因:。
②从结构的角度解释脱水后溶解度降低的原因:。
a.主要在阴极室产生
b.在电极上放电,可能产生
c.阳离子交换膜破损导致向阳极室迁移,可能产生
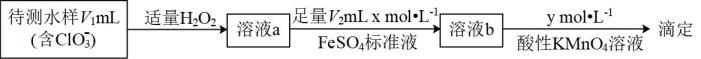
①加入的目的是消耗水样中残留的
和
。若测定中未加入
, 则测得的水样中
的浓度将(填“偏大”“偏小”或“不受影响”)。
②滴定至终点时消耗酸性
溶液,水样中
的计算式为。
①反应的离子方程式为。
②处理时,盐酸可能的作用是:
i.提高 , 使
氧化性提高或
还原性提高;
ii.提高 , 。
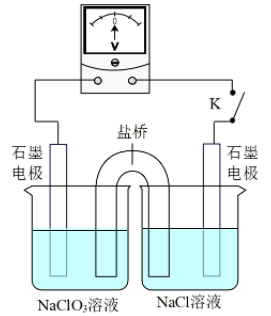
③用如图装置验证i,请补全操作和现象:闭合K,至指针读数稳定后,。
①用硫酸和可溶解软锰矿,请补全该反应的离子方程式:
□+□ +□ =□
+□
□
②浸出时可用代替硫酸和
。下列说法正确的是(填序号)。
a.在反应中作氧化剂
b.用浸出可减少酸的使用
c.该法可同时处理烟气中的 , 减少大气污染
①软锰矿浸出液中的、
可通过加碱转化为沉淀去除,分离出清液的方法是。
②为减少碱用量,可以通过稀释浸出液除去 , 结合离子方程式解释原理:。
在一定空气流速下,相同时间内热解产物中不同价态
的占比随热解温度的变化如图。
热解过程中涉及如下化学反应:
i.
ii.
iii.

①为了增大产物中的占比,可以采用的措施是(答出两条)。
②温度升高,产物中的占比降低,可能的原因是。
【设计实验】
|
序号 |
|
|
|
反应温度/℃ |
|
① |
2.0 |
2.0 |
0 |
20 |
|
② |
2.0 |
1.0 |
1.0 |
20 |
a.盐酸 b.硫酸 c.草酸
小组同学将溶液pH调至1并进行实验①和②,发现紫色并未直接褪去,而是分成两个阶段:
i.紫色溶液转变为青色溶液,ii.青色溶液逐渐褪至无色溶液。
资料:(a)无色,在草酸中不能形成配合物;
(b)无色,有强氧化性,发生反应
(青绿色)后氧化性减弱;
(c) 呈绿色,在酸性条件下不稳定,迅速分解产生
和
。
乙同学从氧化还原角度推测阶段i中可能产生 , 你认为该观点是否合理,并说明理由:。
进一步实验证明溶液中含有 , 反应过程中
和
浓度随时间的变化如下图。

第i阶段中检测到有气体产生,反应的离子方程式为。
上述实验涉及的反应中,草酸的作用是。
结论:反应可能是分阶段进行的。草酸浓度的改变对不同阶段反应速率的影响可能不同。
a.由A制备B时,需要使用浓硝酸和浓硫酸
b.D中含有的官能团只有硝基
c.D→E可以通过取代反应实现
ii. +R3-NH2
+R3-NH2
iii.亚胺结构( )中
)中键性质类似于羰基,在一定条件下能发生类似i的反应。
M与L在一定条件下转化为Y的一种路线如下图。

写出中间产物1、中间产物2的结构简式:、。