 B . 硫磺
B . 硫磺  C . 甲醛
C . 甲醛  D . 浓硫酸
D . 浓硫酸 
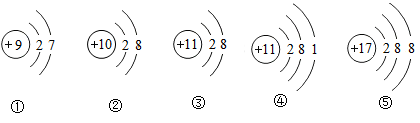
| 选项 | 事实 | 解释 |
| A | 水银温度计放入热水中,水银柱升高 | 受热后原子之间的间隔变大 |
| B | 金刚石硬度很大,石墨却很软 | 构成两种物质的原子不同 |
| C | 蔗糖溶液不导电 | 溶液中没有自由移动的带电粒子 |
| D | 化学反应前后各物质质量总和不变 | 反应前后原子的种类、数目、质量均不改变 |

 图①红磷燃烧过程中弹簧夹未夹紧,则测得空气中氧气的体积分数偏大
B .
图①红磷燃烧过程中弹簧夹未夹紧,则测得空气中氧气的体积分数偏大
B .  图②加入氧化钙后,石灰水中溶质质量减小,会导致玻璃弯管左侧液面降低
C .
图②加入氧化钙后,石灰水中溶质质量减小,会导致玻璃弯管左侧液面降低
C .  图③滴入浓硫酸后,气球胀大,说明氢氧化钠和硫酸反应放热
D .
图③滴入浓硫酸后,气球胀大,说明氢氧化钠和硫酸反应放热
D .  图④通入CO2后,碳酸钠溶液变浑浊,说明氯化钙溶液与碳酸钠溶液发生
图④通入CO2后,碳酸钠溶液变浑浊,说明氯化钙溶液与碳酸钠溶液发生
|
营养素 |
水分 |
蛋白质 |
油脂 |
X |
维生素 |
钙、铁、锌等 |
|
质量 |
92.5g |
0.7g |
0.2g |
6.1g |
6.8mg |
17.1mg |
“X”是指六大基本营养素中的。
请指出使用塑料的利与弊(各写出一条)。
①利:。
②弊:。
如图实验可用来验证可燃物燃烧的条件。

a.将一定量的白磷浸入80℃热水中,白磷不燃烧。
b.将一定量的红磷浸入80℃热水中,红磷不燃烧。
c.升高右侧漏斗至红磷露出水面,红磷不燃烧。
d.升高左侧漏斗至白磷露出水面,白磷燃烧。
①c中红磷不燃烧的原因是。
②对比a和d,可验证可燃物燃烧的条件是。
|
实验操作 |
实验现象及结论 |
任写一个有关反应的化学方程式 |
|
。 |
。 |
。 |
①计算:配制150g质量分数为6%的H2O2溶液,需要质量分数为30%(密度为1.1g/cm3)的H2O2溶液体积为mL(计算结果保留一位小数),水为g。
②量取:用量筒量取所需H2O2溶液和水,倒入烧杯中。用量筒量取液体时,视线应与。
③混匀:…。

①实验室用氯酸钾(MnO2作催化剂)制取干燥的氧气,选择的发生装置和收集装置为(填字母),反应的化学方程式为。
②实验室用发生装置B制取氧气的化学方程式为。
①若其他操作正确,量取水时俯视读数,则配制的H2O2溶液溶质质量分数6%(填“>”、“<”或“=”)。
②若用E装置收集一瓶(容积为200mL)体积分数为80%的氧气,预先应用量筒量取mL的水加入该集气瓶中(不考虑水蒸气的影响)。

①小明设计了如图所示方案。根据现象,得出铜、锌、银三种金属的活动性由强到弱的顺序为。发生反应的化学方程式为。
②小芳选择了光亮的铜丝、溶液和溶液(均写化学式)也验证出铜、锌、银三种金属的活动性顺序。

【资料】
①SiO2既不溶于水也不溶于酸。
②煅烧时发生的反应为: 。


【查阅资料】
①碱式碳酸亚铁受热完全分解生成氧化亚铁、二氧化碳和水。
②氧化亚铁不稳定,在空气中加热会被氧化成四氧化三铁。
①检查装置气密性后,称取4.83g碱式碳酸亚铁粉末放在装置B中,连接仪器。
②打开弹簧夹K,鼓入一段时间空气,称量装置C、D、E的质量。
③关闭弹簧夹K,加热装置B,直至观察到装置C中,再打开弹簧夹K,缓缓通入空气一段时间,这样操作的目的是。
④再次称量装置C、D、E的质量。
|
装置C/g |
装置D/g |
装置E/g |
|
|
加热前 |
200.00 |
180.00 |
180.00 |
|
加热后 |
200.27 |
181.32 |
180.00 |
【实验结论】
在xFeCO3·yFe(OH)2 , x:y=。
①写出装置A中发生反应的化学方程式为。
②实验结束后,装置B中残留固体可能有氧化亚铁、四氯化三铁。
①残留固体可能有四氧化三铁的原因是(用化学方程式表示)。
②称得残留固体的质量为3.36g,通过计算得出残留固体为。