 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 过滤
C . 过滤  D . 检查装置气密性
D . 检查装置气密性 

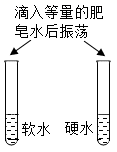 B . 比较黄铜和铜的硬度
B . 比较黄铜和铜的硬度 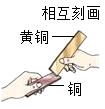 C . 验证燃烧需要氧气
C . 验证燃烧需要氧气 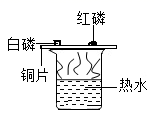 D . 探究铁锈蚀的条件
D . 探究铁锈蚀的条件 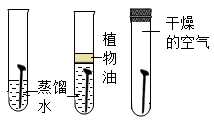

①Ⅱ中反应为CO2+C 2CO,其中化合价发生改变的元素是。
②Ⅲ中一氧化碳与赤铁矿反应的化学方程式为。
①计算并称量:用托盘天平称量7.5g氯化钠固体,用量筒量取mL水。
②溶解:溶解时需要用到玻璃棒,它的作用是。
③下列实验操作中,会引起溶质质量分数偏差的有。
A.称量药品时,药品和砝码放反 B.量取水时俯视读数 C.装瓶时洒出少量溶液

①烧杯①中溶液的质量为。
②上述溶液为饱和溶液的是(填烧杯序号)。
③能将不饱和KCl溶液变为饱和KCl溶液的方法正确的是(填序号,下同)。
A.升高温度 B.加水 C.加KCl固体 D.倒出部分溶液
④烧杯④中溶液的溶质质量分数约为。
A.26% B.29% C.35% D.40%


|
类别 |
X牙膏 |
Y牙膏 |
|
摩擦剂 |
碳酸钙 |
二氧化硅 |
|
摩擦剂的物质类别 |
|
|
根据你的推测,牙膏摩擦剂在水中的溶解性是(填“易溶”或“难溶”)

①M的俗称是;证明M中含有未烧透的石灰石最简单的方法是(填字母序号,下同)。
A.加热 B.滴加稀盐酸 C.加水溶解 D.加入氢氧化钠溶液
②Ⅰ、Ⅱ、Ⅲ反应中,写出属于复分解反应的化学方程式。
[注:装置C中相关反应的化学方程式为: ]

①装置A中发生反应的化学方程式为,反应结束后,还要持续通一段时间空气的目的是。
②图中D处还应该连接一个装置,该装置的作用是。
A.尾气处理 B.干燥 C.吸收空气中的二氧化碳
③下列各项措施中,能提高测定准确度的是。
A.滴加盐酸不宜过快
B.把盐酸换成不具有挥发性的硫酸
C.在装置A~B之间增添盛有浓硫酸的干燥装置
D.在装置B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
④实验中准确称取8.0 g样品三份,进行三次测定。通过过滤、干燥、称量得出生成BaCO3的平均质量,再通过化学方程式计算,得出装置B中反应生成CO2的平均质量为0.44 g,则样品中碳酸钙的质量分数为。
⑤有同学认为不必测定C中生成的BaCO3质量,只需测定装置C吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。你认为按此方法测定的结果会怎样?(填“偏大”、"偏小”或“无影响”),原因是什么?。
【准备的物品】:食用醋精、食盐、纯碱、紫甘蓝汁、氯化钙除湿剂(某品牌)、生锈铁钉、pH试纸(带标准比色卡)、筷子。
【资料1】①食用醋精中含有10%~15%的醋酸,呈无色。
②氯化钙除湿剂是易溶于水的白色固体,水溶液无色、显中性;氯化钙可与纯碱发生反应: 。(除湿剂的其它成分不参与反应)
③紫甘蓝汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝色。
|
实验步骤 |
实验现象 |
实验结论 |
|
①将紫甘蓝汁液滴入醋精中 |
溶液变成色 |
酸能与指示剂反应 |
|
②将生锈铁钉放入醋精中 |
铁锈逐渐消失,溶液变为色,一段时间后有气泡冒出 |
酸能与某些金属氧化物反应,酸能与某些反应 |
|
③将醋精加入纯碱中 |
有气泡冒出 |
酸能与碱反应 |
①小明认为步骤③不能得到“酸能与碱反应”的结论,理由是。
②小亮想利用pH试纸进一步测定醋精的酸碱度,在实验中他用到了筷子,该实验中“筷子”能替代实验仪器中的。
【资料Ⅱ】①水、氯化钠溶液均为中性;Cl-对溶液的酸碱性没有影响。
②Na2CO3在水中全部电离生成Na+和 。
参考分析资料Ⅰ和资料Ⅱ的信息后,小晶利用上面准备的药品,按如图流程进行实验。

【交流表达Ⅱ】
X水溶液溶质的化学式为,加入X溶液的目的是。