|
|
|
|
A.返回舱与推进舱分离时使用的推进剂——液氧和液氢 | B.航天员返回途中穿着的航天服——合成纤维及尼龙膜 | C.返回舱减速伞材料——高强度锦纶纤维 | D.返回舱侧壁壳体——高强度铝合金 |
 C . 基态磷原子的轨道表示式:
C . 基态磷原子的轨道表示式:选项 | 事实 | 推测 |
A | Na、Al能够与盐酸反应置换出H2 | Mg也一定能与盐酸反应置换出H2 |
B | H3PO4是中强酸,H2SO4是强酸 | HClO4是强酸 |
C | Si是半导体材料,Ge也是半导体材料 | IVA族元素的单质都是半导体材料 |
D | Ca与冷水较易反应,Mg与冷水较难反应 | Be与冷水更难反应 |
 +H++2e-=
+H++2e-= +Cl-
D . 生成0.1molH2CO3 , 电池反应电子转移数目为0.4mol
+Cl-
D . 生成0.1molH2CO3 , 电池反应电子转移数目为0.4mol
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某盐溶液中先加入氯水,再滴加KSCN溶液 | 溶液变红色 | 一定含有Fe2+ |
B | SO2缓慢通入滴有酚酞的NaOH溶液中 | 溶液红色褪去 | SO2具有漂白性 |
C | 少量Zn粉加入1.0mol/L Fe2(SO4)3溶液中 | 溶液颜色变浅 | 金属Zn比Fe活泼 |
D | 取少量某无色溶液,先滴加氯水,再加入少量CCl4 , 振荡、静置 | 溶液分层,下层呈紫红色 | 原无色溶液中一定有I- |


①不含—CH3
②含2种官能团
③含苯环,且苯环上仅有2个取代基
④核磁共振氢谱有三组吸收峰,峰面积之比为3∶2∶2
 为原料合成
为原料合成温度/℃ | 压强/MPa | 氨的平衡含量 |
200 | 10 | 81.5% |
550 | 10 | 8.25% |
①该反应为(填“吸热”或“放热”)反应。
②哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是。

①曲线a对应的温度是。
②M、N、Q点平衡常数K的大小关系是。

4NH3(g)+3O2(g)2N2(g)+6H2O(g)ΔH=-1268kJ·mol-1
2NO(g)N2(g)+O2(g)ΔH=-180.5kJ·mol-1
请写出NH3转化为NO的热化学方程式。

①H、C、N、O的电负性由大到小的顺序是。
②烟酸中碳原子的杂化方式为。


资料:
ⅰ.VOSO4高温易分解
ⅱ.含磷有机试剂对溶液中离子萃取能力为Fe(III)>V(IV)>V(V)>Fe(II)
ⅲ.含磷有机试剂萃取过程中溶液的H+浓度越高,萃取率越低,萃取钒效果越差
ⅳ.10VO+8H2O
H2V10O
+14H+
ⅴ.氢氧化物完全沉淀时溶液的pH表
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
完全沉淀 | 3.2 | 9.0 | 4.7 |
①请结合相关离子方程式,说明加入Na2SO3的第二个作用。
②解释加氨水调节pH≈5的原因是。

称取ag产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1mLc1mol·L-1(NH4)2Fe(SO4)2溶液(VO+2H++Fe2+=VO2++Fe3++H2O)最后用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知MnO
被还原为Mn2+ , 假设杂质不参与反应。则产品中V2O5的质量分数是。(V2O5的摩尔质量:182g•mol-1)
实验1:
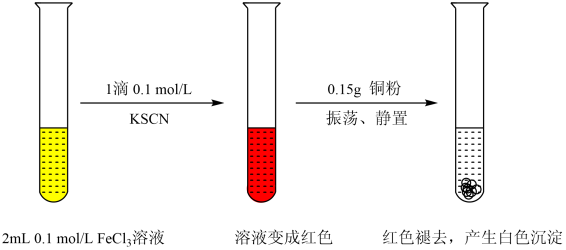
资料:ⅰ.CuSCN、CuCl均为难溶于水的白色固体;均能与硝酸反应,分别生成Cu2+与SO、Cu2+与Cl-。
ⅱ.(SCN)2性质与卤素单质相似,其水溶液呈黄色。

由实验2可知,实验1中白色沉淀的成分是。
|
步骤 |
实验操作 |
实验现象 |
|
I |
|
溶液变为蓝色,澄清透明,底部只有少量红色固体剩余 |
|
II |
取I中上层清液于试管中,滴加1滴0.1mol/L KSCN溶液 |
立刻出现红色,同时有白色沉淀生成 |
|
III |
振荡II中试管,静置 |
白色沉淀变多,红色逐渐褪去 |
①步骤I的实验操作是。
②根据实验3的现象,小组同学认为Fe3+与Cu反应的氧化产物不含Cu(I),他们的判断依据是。
③步骤Ⅱ中加入KSCN溶液后出现红色的可能原因是。
④解释步骤III中实验现象产生的可能原因:。