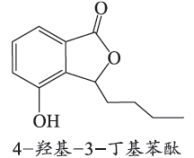

选项 | 实验操作 | 试剂A | 现象 | 结论 |
A |
| 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
B | 新制氯水 | 黄绿色褪去 | SO2具有漂白性 | |
C | H2S溶液 | 出现淡黄色浑浊 | SO2具有氧化性 | |
D | 盐酸酸化的BaCl2溶液 | 无明显变化,一段时间后产生白色沉淀 | 硫元素从+4价被氧化到+6价 |
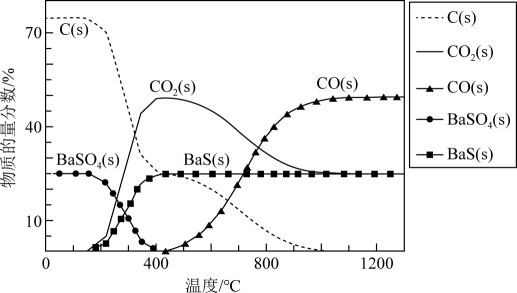
已知:碳热还原BaSO4过程中可能发生下列反应。
i.BaSO4(s)+2C(s)=2CO2(g)+BaS(s) △H1
ii.BaSO4(s)+4C(s)=4CO(g)+BaS(s) △H2=+571.2kJ·mol-1
iii.BaSO4(s)+4CO(g)=4CO2(g)+BaS(s) △H3=-118.8kJ·mol-1
下列关于碳热还原BaSO4过程的说法正确的是( )
资料:i.空燃比是通入空气与燃料质量的比值,按化学计量数反应时的空燃比称为理论空燃比。
ii.2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1
①与完全燃烧相比,每2molC8H18不完全燃烧时少放出的能量为。
②为减少油耗,实际使用过程中的空燃比(填“大于”或“小于”)理论空燃比。
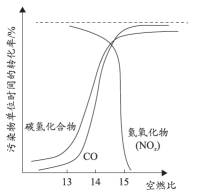
已知:i.空燃比大于15后,空燃比越大,尾气的温度越低。
ii.CO和NO的反应为放热反应。
①三元催化转化器可将CO和NO转化为无害气体,反应的化学方程式为。
②空燃比大于15时,尾气中氮氧化物单位时间的转化率接近于0,可能的原因是。(写出2条)。
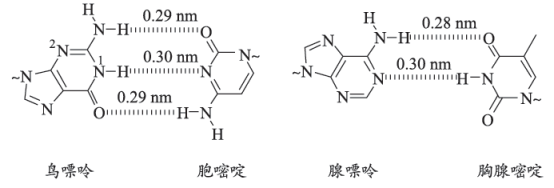
①鸟嘌呤中2号N的杂化类型为。
②鸟嘌呤中N—H键的平均键长。(填“大于”“小于”或“等于”)0.29nm。
①碱基中,O、N能与H形成氢键而C不能,原因是。
②下列说法正确的是(填序号)。
a.氢键的强度较小,在DNA解旋和复制时容易断裂和形成
b.鸟嘌呤与胞嘧啶之间的相互作用比腺嘌呤与胸腺嘧啶之间的更强
c.碱基配对时,一个H可以同时与多个原子形成氢键
①鸟嘌呤异构化后的结构简式为。
②鸟嘌呤异构化后最有可能配对的嘧啶碱基是。。

a.可以发生取代反应、加成反应、氧化反应
b.存在酚类同分异构体
c.可以用酸性KMnO4溶液检验其中的碳碳双键
d.核磁共振氢谱中有6种信号峰,是手性分子
①![]() +
+![]()
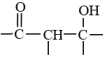
③![]()
![]()
G与L可以在碱性条件下经过如图所示的多步反应得到X。
G+L→中间产物1中间产物2
中间产物3
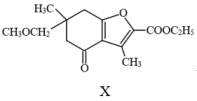
中间产物1、中间产物3的结构简式是、。
已知:PNP的溶解性与苯酚类似,微溶于水;其化学性质稳定,可被•OH、HClO氧化降解为无机物,但不能与O2反应。

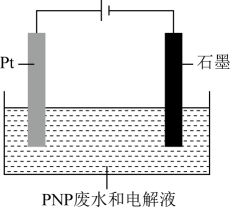
①•OH(氧元素为-1价)由水产生,•OH在(填“Pt”或“石墨”)电极产生。
②产生•OH的电极反应式为。
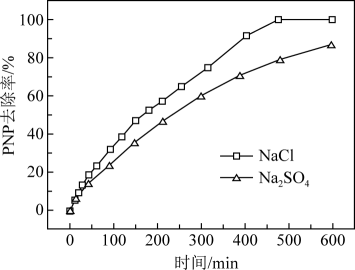
①电解质为NaCl时,阳极副反应的电极反应式为。
②电解质为NaCl时,PNP去除率较Na2SO4高,可能的原因是。
已知:
i.(NH4)2S2O8具有强氧化性,能完全电离,S2O易被还原为SO
;
ii.淀粉检测I2的灵敏度很高,遇低浓度的I2即可快速变蓝;
iii.I2可与S2O发生反应:2S2O
+I2=S4O
+2I-。
|
编号 |
1-1 |
1-2 |
|
实验操作 |
|
|
|
现象 |
无明显现象 |
溶液立即变蓝 |
为了研究(NH4)2S2O8与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
|
编号 |
0.2mol·L-1KI溶液/mL |
0.01mol·L-1Na2S2O3溶液/mL |
蒸馏水/mL |
0.4%的淀 粉溶液/滴 |
0.2mol·L-1(NH4)2S2O8溶液/mL |
变色时间/s |
|
2-1 |
2 |
0 |
2.8 |
2 |
0.2 |
立即 |
|
2-2 |
2 |
0.8 |
0.2 |
2 |
2 |
30 |
猜想1:(NH4)2S2O8先与Na2S2O3反应,使c(S2O)降低;
猜想2:(NH4)2S2O8先与KI反应,..............。
①甲同学提出猜想1的依据:由信息iii推测,Na2S2O3的还原性(填“强于”或“弱于”)KI的。
②乙同学根据现有数据证明猜想1不成立,理由是。
③补全猜想2:。