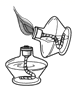
 点燃酒精灯
B .
点燃酒精灯
B . 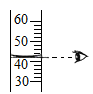 量筒读数
C .
量筒读数
C . 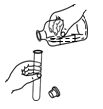 倾倒液体
D .
倾倒液体
D . 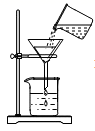 过滤
过滤
编号 | A | B | C | D |
实验方案 |
|
|
|
|
实验目的 | 探究影响物质溶解性的因素 | 探究燃烧条件之一需要可燃物 | 探究铁钉生锈时O2是否参与反应 | 比较Zn和Fe的金属活动性强弱 |
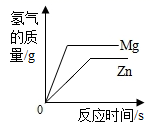 向两份等质量,相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉
B .
向两份等质量,相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉
B . 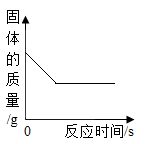 向一定质量二氧化锰固体中加入一定质量的过氧化氢溶液
C .
向一定质量二氧化锰固体中加入一定质量的过氧化氢溶液
C . 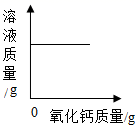 温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙
D .
温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙
D . 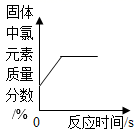 加热一定质量氯酸钾和二氧化锰的固体混合物
加热一定质量氯酸钾和二氧化锰的固体混合物
选项 | 实验目的 | 实验操作 |
除去 | 点燃混合气体 | |
除去 | 加入过量的 | |
鉴别黄金和黄铜 | 取样,滴加稀盐酸,观察现象 | |
除去 | 将混合物在空气中灼烧 |
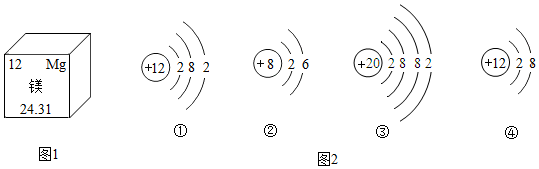
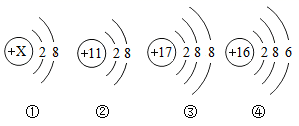
①图为镁在元素周期表中的部分信息,则镁的相对原子质量为 。
②图为几种粒子的结构示意图,其中属于同种元素的是
填序号
, 与镁元素化学性质相似的是
填序号
。
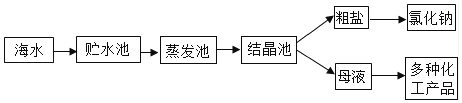
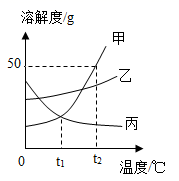
根据海水晒盐的原理,下列说法正确的是____(填序号)。
①需要固体氯化钠的质量g。
②配制过程有以下步骤:a 称量及量取;b 计算;c 溶解;d 装瓶贴标签,正确顺序是 (填序号)。
A.bcad B.bacd
③将 50 g 溶质质量分数为 10%的氯化钠溶液,稀释成 5%的氯化钠溶液,需要加水的g。
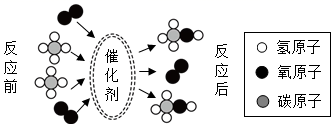
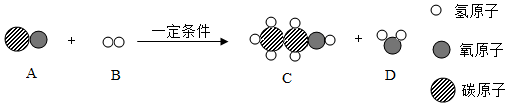
①电解水的化学方程式为。
②电解水的实验证明水是由组成的。
a.面粉b.硝酸钾c.泥沙d.花生油
|
温度/℃ |
0 |
20 |
40 |
60 |
80 |
|
|
溶解度/g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
|
KCl |
27.6 |
34.0 |
40.0 |
45.5 |
51.1 |
|
①20℃时,氯化钠的溶解度为g。
②20℃时,将20g氯化钠固体加入到50g水中,充分溶解,所得氯化钠溶液的质量为g。
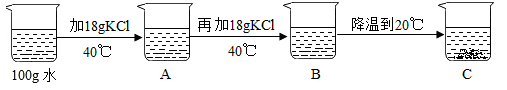
③某同学进行实验如下图所示,得到相应的A、B、C三种溶液,C中析出的氯化钾固体质量为g。
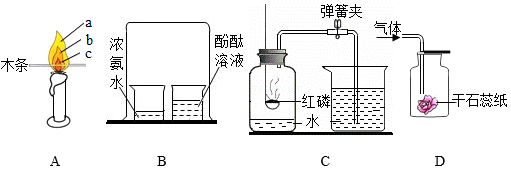
A.红磷过量 B.气密性不好 C.燃烧完成后未冷却到室温打开止水夹
查阅资料: ;
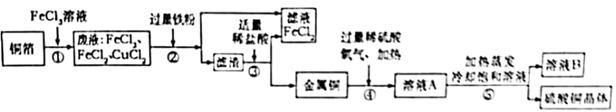
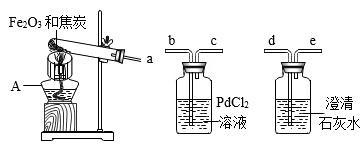
(查阅资料)①铁粉为黑色;常温下,Fe、Fe3O4可被磁铁吸引;
②PdCl2 , 溶液可用于检验CO,原理是∶PdCl2+CO+H2O=Pd↓+CO2+2HCl;
③Fe3O4与硫酸反应∶ Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O。
(实验现象)澄清石灰水变浑浊,PdCl2溶液中产生黑色沉淀,玻璃管内粉末全部变成黑色。冷却后,用磁铁靠近黑色固体,黑色固体被部分吸引。
(实验结论)反应生成CO 和CO2 , 磁铁上的黑色固体可能是 Fe、Fe3O4。
猜想一:Fe
猜想二∶ Fe3O4
猜想三∶ Fe 和Fe3O4
(设计实验)
|
设计思路 |
操作 |
现象 |
结论 |
|
定性实验 |
取少量黑色固体于试管中,加入足量稀硫酸,充分反应 |
固体完全溶解,产生气泡 |
猜想不成立 |
|
定量实验 |
取一定质量的稀硫酸(足量)放入烧杯中,加入5.6g黑色固体,充分反应后称量溶液的质量 |
固体完全溶解,产生气泡,溶液增加的质量为 |
猜想一成立 |
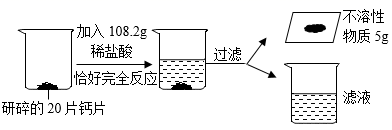
根据图示信息,完成下列各题: