
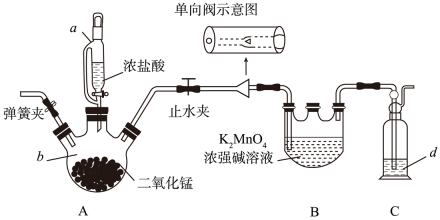
选项 | A | B | C | D |
操作 |
|
|
|
|
实验目的 | 混合浓硫酸和乙醇 | 定容 | 干燥 | 分离碘和酒精 |

第一次 | 第二次 | 第三次 | 第四次 | |
17.30 | 17.90 | 18.00 | 18.10 |
计算试样中过氧化氢的浓度为mol·L-1 .

若“沉铈”中,Ce3+恰好沉淀完全[c(Ce3+)为1.0×10-5mol·L-1 , 此时溶液的pH为5,则溶液中c()= mol·L-1 (保留2位有效数字)。
已知常温下:
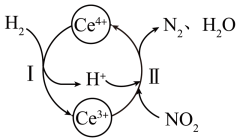
①该反应中的催化剂为(写离子符号);
②该转化过程中还原剂与氧化剂物质的量之比为。

总反应: CO(g) + N2O(g) CO2(g) + N2(g) ∆H= kJ·mol-1; 该总反应的决速步是反应 (填 “①"或“②”),该判断的理由是.
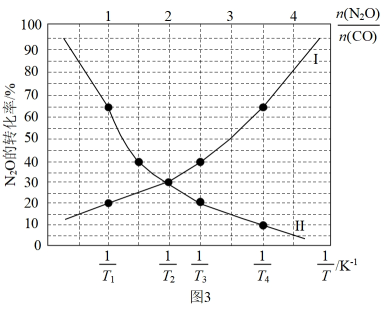
①表示N2O的转化率随的变化曲线为曲线(填“I”或“II”);
②T1T2 (填“>”或“<"),该判断的理由是
③已知:该反应的标准平衡常数 , 其中
为标准压强 (100kPa),p(CO2)、p(N2)、 p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数
= ( 计算结果保留两位有效数字,p分=p总 ×物质的量分数)。

①组成M的5中元素中,除H元素外,另外4种元素第一电离能由大到小的顺序为(填元素符号),其中C原子的杂化类型为。
②图中各微粒不存在的作用力有 ( 填标号)
a. 极性键 b.非极性键 c. 配位键
d. π键 e.离子键 f.氢键
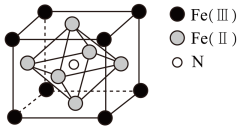
①铁氮化合物的化学式为。
②在该晶胞结构的另一种表示中,N处于顶点位置,则铁处于、位置
③若该化合物密度为pg·cm-3 , 用NA表示阿伏加德罗常数,则由Fe( II )构成的正八面体的体积为cm3
①红外光谱检测分子中含有醛基;
②1H-NMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子。