A.配制一定物质的量浓度的溶液 | B.组成Zn-Cu原电池 | C.实验室制取乙酸乙酯 | D.比较S、C、Si的非金属性强弱 |
|
|
|
|
选项 | 实验操作 | 现象 | 结论 |
A | 将铜片放入盛有稀硝酸的试管中 | 试管口出现红棕色气体 | 铜片与稀硝酸反应产生NO2 |
B | 向盛有无色透明溶液的试管中滴加澄清石灰水 | 生成白色沉淀 | 溶液中一定存在 |
C | 向盛有少量蔗糖的烧杯中加入几滴水,再加入适量浓硫酸,搅拌 | 蔗糖变黑,体积膨胀,产生有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
D | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升华 |
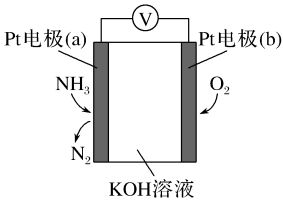


请回答下列问题:
该反应的化学反应方程式为。
①
②
请回答下列问题:
下列措施可以加快反应②的速率的是____。

①试剂a为(填化学式,下同),滤渣II的主要成分为。
②在过滤操作中要使用玻璃棒,其作用是。
③检验滤液I中是否存在Fe3+的试剂是。
④制备的反应原理是:
当反应中转移电子总数约为
时,则生成
的物质的量为mol。