 加水和面
B .
加水和面
B .  剁肉拌馅
C .
剁肉拌馅
C .  擀皮包饺子
D .
擀皮包饺子
D .  烧火煮饺子
烧火煮饺子
 B . 称量固体
B . 称量固体  C . 粉末状固体取用
C . 粉末状固体取用  D . 液体加热
D . 液体加热 

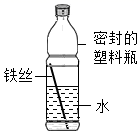
①一段时间后,铁丝会由下向上出现锈蚀现象
②一段时间后,水面处铁丝锈蚀最严重
③铁锈的主要成分是四氧化三铁
④一段时间后,塑料瓶可能会变瘪



7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
15 P 磷 30.97 | 16 S 硫 32.07 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
33 As 砷 74.92 | 34 Se 硒 78.96 | 35 Br 溴 79.90 | 36 Kr 氪 83.80 |





【选择仪器】组装发生与收集装置(要求:可以随时控制反应速率),在以上装置中选择(填序号);
【步骤一】
把六种金属分别放入中,根据是否能够发生反应,分成两组分别进行实验。
最简单的实验操作,可以把两根不同的金属丝,同时放入一种金属化合物的溶液中,观察是否反应,即可比较出这三种金属的活动性铜>银>金。这种金属化合物的溶液是:;
实验操作 | 现象 | |
实验一 | 将镁条插入硫酸锌溶液 | 镁条表面有固体析出 |
实验二 | 将铝丝插入硫酸锌溶液 | 铝丝表面有固体析出 |
实验三 | 将铁丝插入硫酸锌溶液 | 无明显现象 |
镁条插入硫酸锌溶液中发生反应的化学方程式为:;
实验四 |
现有硝酸铝、硝酸锌、氯化亚铁、硫酸铜四种溶液和一种未知金属(该金属是金属活动顺序表中的一种金属),以及必要的实验仪器。
分组选择物质进行实验:
实验过程 | 判断是否发生反应 | |
实验五 | 将未知金属放入Al(NO3)3溶液 | 不反应 |
实验六 | 将未知金属放入Zn(NO3)2溶液 | 不反应 |
实验七 | 将未知金属放入FeCl2溶液 | 发生反应 |
实验八 | 将未知金属放入CuSO4溶液 | 发生反应 |
结论:该金属是;