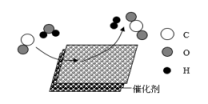
 B .
B . 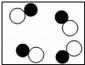 C .
C .  D .
D . 





a.加碘盐;b.冰水混合物;c.硫磺;d.硫酸铝钾晶体[KAl(SO4)2·12H2O];e.KClO3;
f.钢; g.稀硫酸 h.金刚石
混合物 单质

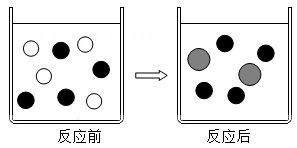

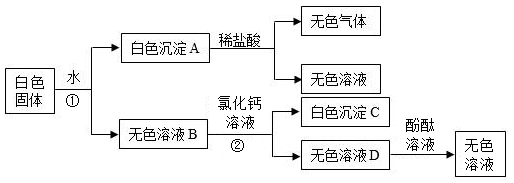
请回答下列有关问题:

①;
②。
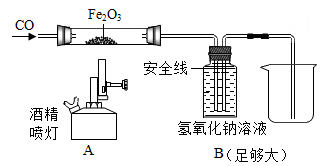
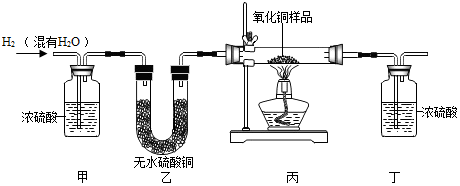
⑴取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液。
⑵取实验⑴滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体。则原白色 粉末中一定含有。
CaCO3 ⑶为了进一步探究白色粉末的组成,取是按 (1)得到的滤液,向其中通入CO2 , 产生白色沉淀,则原白色粉末中一定还含有。

该反应的基本类型属于。

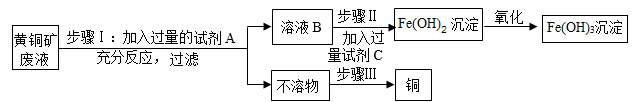
|
氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Al(OH)3 |
|
|
开始沉淀时的pH |
2.3 |
4.0 |
开始溶解时的pH |
7.8 |
|
完全沉淀时的pH |
3.7 |
5.2 |
完全溶解时的pH |
10.8 |
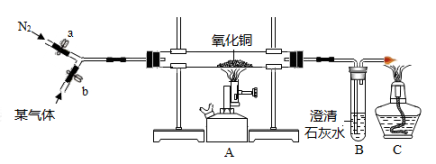

【查阅资料】①SO2 能使品红溶液褪色;②SO2 易与高锰酸钾溶液反应而被吸收,并能使其褪色;③SO2 能使氢氧化钡溶液和澄清石灰水变浑浊;④CO和CO2均不能使品红溶液褪色,也不与高锰酸钾溶液反应。
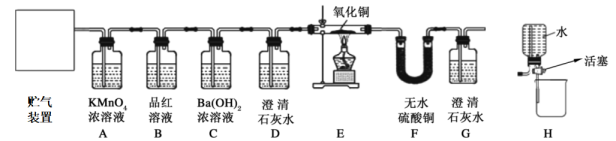
【实验分析】
若装置按照D→A→B→D→E→F→G连接,并观察到以下现象
|
装置 |
D |
A |
B |
D |
E |
F |
G |
|
现象 |
变浑浊 |
褪色 |
无现象 |
变浑浊 |
变红 |
变蓝 |
变浑浊 |
由现象可以确定一定存在的气体有。
|
氢氧化物 |
Fe(OH)3 |
Mg(OH)2 |
|
开始沉淀的 pH |
1.5 |
8.6 |
|
完全沉淀的 pH |
3.2 |
11.1 |