 B . 称量固体 NaOH
B . 称量固体 NaOH  C . 氢气还原氧化铜
C . 氢气还原氧化铜  D . 测溶液的酸碱度
D . 测溶液的酸碱度 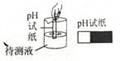
| | | | |
| A. | B. | C. | D. |
| 选项 | 实验目的 | 实验操作 |
| A | 检验溶液中含铵根离子 | 取样,加入氢氧化钠,微热,闻气味 |
| B | 除去CO2气体中少量HCl气体 | 通过NaOH溶液 |
| C | 检验废水中是否含有 | 滴加BaCl2溶液 |
| D | 鉴别溶液:NaCl、Na2CO3、HCl、KNO3 | 将组内物质相互混合,观察现象 |


选项 | 性质 | 用途 |
A | 氢氧化钙呈碱性 | 改良酸性土壤 |
B | 浓硫酸具有脱水性 | 干燥氧气 |
C | 稀盐酸能与某些金属氧化物反应 | 除铁锈 |
D | 氢氧化钠能与某些非金属氧化物反应 | 吸收二氧化硫 |
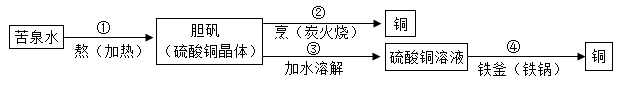


①将固体溶于水得无色透明溶液,加入足量BaCl2溶液,过滤后得到5克白色沉淀。
②在沉淀中加入过量稀硝酸,仍有3克白色沉淀。
③在滤液中滴加AgNO3溶液,产生白色沉淀。
则

①试管中的铁钉最易生锈.
②比较两组试管中产生的实验现象可知,钢铁锈蚀需要氧气的参与;
③铁锈是红棕色的固体,属于(纯净物、混合物),它的主要成分是。铁锈是一种疏松多孔的物质,会加快铁的锈蚀,家庭使用的铁锅防锈的方法是.

【查阅资料】
一定温度下,CH4可将 Fe2O3 还原为单质铁。若温度控制不当,还可生成少量的 Fe3O4。
【实验探究】
进行研究.
【收集资料】
通过阅读标签及查阅资料,她获得如下信息:
⑴该固体酒精中含有酒精、氯化钙、氢氧化钠三种物质;
⑵酒精的化学式为 C2H5OH; (3)氯化钙、氯化钡的水溶液均呈中性.
【提出问题】
⑶酒精的化学式与 NaOH 相比,都有“OH”,那么酒精的水溶液是不是显碱性?
⑷固体酒精中的氢氧化钠是否变质及变质的程度如何?
实验一:她取少量酒精溶液于试管中,滴加硫酸铜溶液,未观察到蓝色沉淀,说明酒精溶液(填“显”或“不显”)碱性.
除去部分变质的氢氧化钠溶液中的杂质,方法是(用化学方程式表示).

| 装置丙 | 装置丁 | |
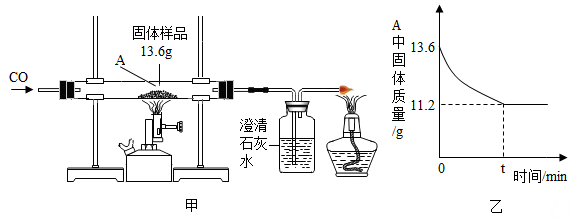
| 反应前 | 48.8 克 | 161.2 克 |
| 反应后 | 46.5 克 | 163.9 克 |
小明根据装置丙减少的质量就是氧元素质量,求得氧化铜的质量为 11.5 克,纯度为76.7%.小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度
|
实验编号 |
1 |
2 |
3 |
|
实验操作 |
| | |
实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁…,应该可以从中提炼出铁和铜.经思考后,他设计了如图所示的实验.


|
实验 |
1 |
2 |
3 |
4 |
|
加样品的质量(g) |
5 |
10 |
15 |
20 |
|
生成CO2的质量(g) |
1.76 |
3.52 |
4.4 |
m |
问:
