 过滤
C .
过滤
C .  测溶液pH
D .
测溶液pH
D .  稀释浓硫酸
稀释浓硫酸
①银汞合金是一种新型化合物
②银汞合金是一种金属材料
③银汞合金的硬度比锡的大
④银汞合金的毒性一定远低于汞的毒性
⑤组成银汞合金的各成分之间发生了化学反应

①铁锈的主要成分是四氧化三铁
②一段时间后,塑料瓶可能会变瘪
③一段时间后,水面处铁丝锈蚀最严重
④一段时间后,铁丝会由下向上出现锈蚀现象
 用方案甲探究同种物质在不同溶剂中的溶解性
B .
用方案甲探究同种物质在不同溶剂中的溶解性
B .  用方案乙探究空气是铁生锈的必要条件
C .
用方案乙探究空气是铁生锈的必要条件
C .  用方案丙探究不同催化剂对H2O2分解速率的影响
D .
用方案丙探究不同催化剂对H2O2分解速率的影响
D .  用方案丁探究合金及其成分金属的熔点高低
用方案丁探究合金及其成分金属的熔点高低

 B . 向等质量的Mg和Al中分别加入足量相同溶质质量分数的稀盐酸
B . 向等质量的Mg和Al中分别加入足量相同溶质质量分数的稀盐酸 C . 向等质量的Mg和MgO中分别加入足量相同溶质质量分数的稀硫酸
C . 向等质量的Mg和MgO中分别加入足量相同溶质质量分数的稀硫酸 D . 向一定质量的稀H2SO4和MgSO4的混合溶液中逐滴加入Ba(OH)2溶液
D . 向一定质量的稀H2SO4和MgSO4的混合溶液中逐滴加入Ba(OH)2溶液
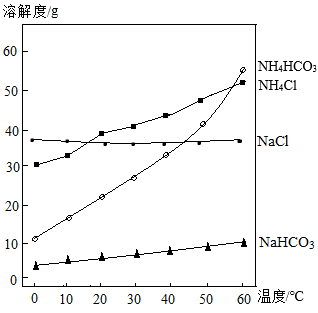


①用图1中仪器完成实验,还缺少的玻璃仪器是(填名称),玻璃棒在实验中的作用是。
②配制该溶液需要g水。用量筒量取水时,俯视读数会导致所配溶液的溶质质量分数10%。(填“大于”或“小于”)
①中溶液变为红色(填“试管1”或“试管2”)。
②试管3中产生现象是,试管4中无明显现象,由此推断金属活动性Cu比Zn(填“强”或“弱”)。试管3中发生反应的化学方程式为。
③试管5中生成一种盐和两种氧化物,该反应的化学方程式为。
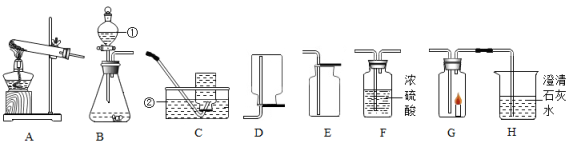
a、能与水反应 b、能与空气中的某些成分发生反应 c、密度与空气接近
①Na2CO3 ②BaCl2 ③NaOH
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。

a、氢氧化钾溶液滴入稀硫酸中 b、稀硫酸滴入氢氧化钾溶液中
【猜想与假设】
猜想一:只有K2SO4 ; 猜想二:有K2SO4和H2SO4; 猜想三:有K2SO4和KOH
同学们讨论后一直认为猜想三是错误的,理由是。
为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取少量反应后的溶液于试管中,加入Fe2O3粉末。 | ① | 溶液中有H2SO4 , 猜想二正确。 |
方案二 | 取少量反应后的溶液于试管中,滴加BaCl2溶液。 | ②产生白色沉淀 | 溶液中有H2SO4 , 猜想二正确。 |
【实验结论】通过探究,同学们一致确定猜想二是正确的。
①丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是。
②方案一中的Fe2O3粉末可以用下列的某些物质代替,也能得到同样的实验结论,请你选出可用药品的字母序号。
A.Mg B.CuO C.KCl D.Na2CO3
③验证猜想也可以取少量反应后的溶液于试管中,加入下列药品中的(填序号)。
A.酚酞试液 B.石蕊试液 C.MgCl2 D.Na2CO3
小静同学对小文同学自制发热包的成分进行探究。
小静取适量自制发热包中的固体放入盛有水的烧杯中,迅速放出大量的热,她认为是固体样品中的生石灰与水发生反应产生了热量。为了进一步确认发热包中物质的成分,小静把烧杯中的物质过滤,得到滤液A和滤渣B。
实验步骤 | 实验操作 | 实验现象 | 分析与结论 |
① | 取适量滤渣B放入烧杯中 | 观察到滤渣B慢慢出现红棕色固体,触摸烧杯外壁感到微热并持续了较长时间 | 红棕色固体是 |
② | 取适量滤液A放入试管中,加入过量的氯化钡溶液 | 有白色沉淀生成 | 发热包中除含有生石灰外,一定还含有的物质是 |
③ | 取②中的白色沉淀放入试管中,加入足量的稀硝酸 | 白色沉淀全部溶解,有气泡产生 | |
④ | 取②反应后的上层清液放入试管中,先加入足量稀硝酸,再滴入适量AgNO3溶液 | 有白色沉淀生成 | |
⑤ | 取适量滤渣B放入试管中,加入足量的稀盐酸 | 固体部分溶解,溶液呈浅绿色,有气泡产生 |
步骤②反应后的上层清液中含有的离子共有种。