 过滤
C .
过滤
C .  测溶液pH
D .
测溶液pH
D .  稀释浓硫酸
稀释浓硫酸
①银汞合金是一种新型化合物
②银汞合金是一种金属材料
③银汞合金的硬度比锡的大
④银汞合金的毒性一定远低于汞的毒性
⑤组成银汞合金的各成分之间发生了化学反应



 表示向pH=1的盐酸中不断加入NaOH溶液至过量
B .
表示向pH=1的盐酸中不断加入NaOH溶液至过量
B .  某温度时,向一定量的饱和氢氧化钙溶液中加入少量CaO,再恢复到原温度
C .
某温度时,向一定量的饱和氢氧化钙溶液中加入少量CaO,再恢复到原温度
C .  向盛有一定质量NaOH和Na2CO3混合溶液的烧杯中滴加稀盐酸至过量
D .
向盛有一定质量NaOH和Na2CO3混合溶液的烧杯中滴加稀盐酸至过量
D . 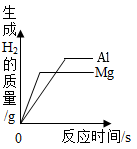 向等质量的Mg和Al中分别加入足量相同溶质质量分数的稀盐酸
向等质量的Mg和Al中分别加入足量相同溶质质量分数的稀盐酸


①浓硫酸、浓盐酸应当密封保存,原因是。
②铁桶能存放氢氧化钠溶液,不能存放稀盐酸。原因是(用方程式表示)。
①盐酸常用于除去铁制品表面的锈,反应的化学方程式是。使用盐酸时要小心,不小心溅到了手上,应当立即,再涂上3%-5%的碳酸氢钠溶液。
②下列物质中可用作治疗胃酸过多的胃药有(填序号)。
A.Al(OH)3 B.CaCO3粉末 C.NaCl D.NaOH E.CuO
写出上述胃药中碱与胃酸反应的化学方程式,选择一种不能治疗胃酸过多的物质,说明不能使用的理由。
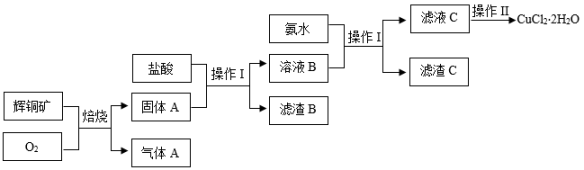
【查阅资料】:Fe3+、Cu2+转化为对应的碱时,溶液的pH的数轴关系如下图:

①调节溶液的pH,控制的范围是3.2≤pH<,使Fe3+完全转化为Fe(OH)3沉淀;
②。
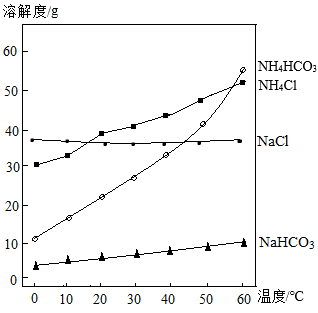
A.CuCl2的溶解度随温度升高变化较大 B.溶液C中两物质的密度不同
C.NH4Cl的溶解度随温度升高变化不大 D.溶液C中两物质的颜色不同
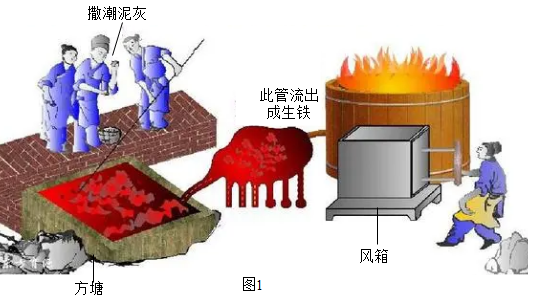

根据图文回答下列问题。
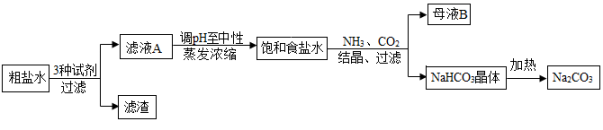
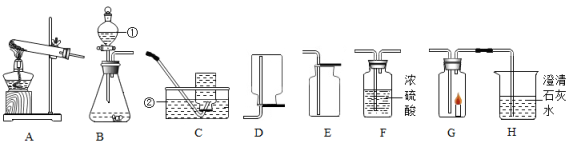
a、能与水反应 b、能与空气中的某些成分发生反应 c、密度与空气接近
①【提出问题】。
【提出猜想】猜想1:KOH溶液中的H2O使无色酚酞试液变红;
②猜想2:KOH溶液中的K+使无色酚酞试液变红;
猜想3:。
③【实验探究】
实验操作 | 实验现象 | 结论 |
①用试管取少量蒸馏水,滴入1~2滴无色酚酞试液 | 试管内溶液不变色 | 猜想1不成立 |
②用试管取少量KCl溶液,滴入1~2滴无色酚酞试液 | 猜想2不成立 | |
③,滴入1~2滴无色酚酞试液 | 试管内溶液变红 |
④【讨论反思】有同学认为猜想1不需要实验验证就可以排除,你认为该同学的理由是:。
⑤【拓展提高】向Ba(OH)2溶液中滴入几滴无色酚酞试液,观察到的现象是。
【实验用品】pH试纸、Zn片、氧化铜粉末、稀H2SO4、NaOH溶液、BaCl2溶液。
【假设猜想】猜想一:Na2SO4
猜想二:Na2SO4、NaHCO3
猜想三:Na2SO4、H2SO4
①【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据现象或结论填空。
实验方案 | A | B | C | D |
实验操作 |
|
|
|
|
实验现象 | 无气泡产生 | 产生白色沉淀 | ||
实验结论 | 猜想三正确 | 猜想三正确 | 猜想三正确 |
【得出结论】猜想三正确
②【评价反思】老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在的两处明显错误,分别是:
①。
②。
③【总结提高】依据所给实验用品,你还有什么不同方法确认猜想三是正确的。请写出你的实验方案及现象。
【提出问题】镁条表面的灰黑色物质是什么?
【猜想与假设】同学们根据空气的成分对镁条表面的灰黑色物质提出以下猜想:
猜想一:是MgO
猜想二:是MgCO3
猜想三:是Mg(OH)2
猜想四:是Mg2(OH)2CO3
实验小组的小军同学认为灰黑色物质是氧化镁,但是遭到了其他同学的一致反对,
实验序号 | 实验操作 | 实验现象 | 分析与结论 |
实验Ⅰ | 取一定量的灰黑色物质于试管中,滴加稀盐酸,将生成的气体通入澄清石灰水 | 试管中固体溶解,有气泡产生。生成的气体使澄清石灰水变浑浊 | 生成的气体是
|
实验Ⅱ | 另取一定量干燥的灰黑色物质于试管中,加热,将生成的气体依次通过无水硫酸铜和澄清石灰水 | 一段时间后,试管中的灰黑色物质变为白色,无水硫酸铜变为蓝色,澄清石灰水变浑浊 | 无水硫酸铜变为蓝色,说明产物中一定有
|
镁条表面的灰黑色物质是镁与空气中的氧气、共同作用,发生一系列化学反应形成的。为了防止镁条表面形成灰黑色物质,工业上往往将镁和铝制成合金。现有一块21g的镁铝合金与足量的稀硫酸充分反应,生成2g氢气,则这块镁铝合金中镁的质量是 g。
小静同学对小文同学自制发热包的成分进行探究。
小静取适量自制发热包中的固体放入盛有水的烧杯中,迅速放出大量的热,她认为是固体样品中的生石灰与水发生反应产生了热量。为了进一步确认发热包中物质的成分,小静把烧杯中的物质过滤,得到滤液A和滤渣B。
实验步骤 | 实验操作 | 实验现象 | 分析与结论 |
① | 取适量滤渣B放入烧杯中 | 观察到滤渣B慢慢出现红棕色固体,触摸烧杯外壁感到微热并持续了较长时间 | 红棕色固体是 |
② | 取适量滤液A放入试管中,加入过量的氯化钡溶液 | 有白色沉淀生成 | 发热包中除含有生石灰外,一定还含有的物质是 |
③ | 取②中的白色沉淀放入试管中,加入足量的稀硝酸 | 白色沉淀全部溶解,有气泡产生 | |
④ | 取②反应后的上层清液放入试管中,先加入足量稀硝酸,再滴入适量AgNO3溶液 | 有白色沉淀生成 | |
⑤ | 取适量滤渣B放入试管中,加入足量的稀盐酸 | 固体部分溶解,溶液呈浅绿色,有气泡产生 |
①步骤②反应后的上层清液中含有的离子共有种。
②步骤④中生成白色沉淀的化学方程式是。(任写一个)
③发热包中的物质使用前必须保存,使用后注意合理回收。
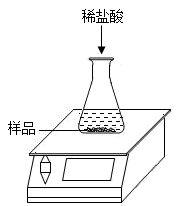
加入稀盐酸的质量/g | 80 | 120 | 160 | 200 |
锥形瓶中物质的质量/g | 100.6 | 138.4 | 176.2 | 216.2 |
试求: