
A | B | C | D | |
实 验 装 置 |
硫在氧气中燃烧 |
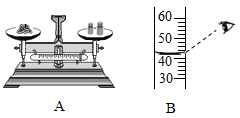
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
排水法收集氧气 |
解 释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积 的变化得出O2的体积 | 集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂 | 集气瓶中的水:水先将集气瓶内空气排尽,后便于观察氧气何时收集满 |
选项 | A.电解水实验 | B探究燃烧的条件 | C.测量空气中氧气的含量 | D.检查装置气密性 |
实验内容 |
|
|
|
|
解释 | 在化学变化中,分子的种类可以发生改变 | ①白磷燃烧②白磷不燃烧,说明可燃物燃烧温度要达到着火点 | 气体体积改变,压强改变,通过测量量筒中水的变化得出氧气的体积 | 装置内气体分子间间隔受热变大 |

A铜+氧气 氧化铜 B氨气+氧气
一氧化氮+水
C氨气+氯化氢→氯化铵 D甲烷+氧气 二氧化碳+水

阅读分析,解答问题:


①该实验利用了铜片的性。
②能验证“可燃物燃烧需要温度达到着火点”的现象是。
A.b处火柴头燃烧,a处火柴头不燃烧
B.b处火柴头燃烧,c处火柴梗不燃烧
C.a处火柴头不燃烧,c处火柴梗不燃烧
①装置A中反应前后,二氧化锰的不变。
②能直接验证质量守恒定律的实验装置是(填字母)。
①下图表示电解水的微观示意图,请在方框内将反应后的微观示意图补充完整。

②若d管中产生气体的质量为32g,则e管中产生气体的质量为g。

三位同学对反应生成的红色固体提出如下猜想:
甲:固体是Cu;乙:固体是;丙:固体是Cu2O和Cu;
【实验】
取红色固体样品,加入适量的稀硫酸,观察到(填实验现象),甲猜想不正确。
①加热时,H2和Cu2O能反应,产生Cu和H2O
②白色的无水CuSO4遇水蒸气会变成蓝色。
为进一步确定红色固体组成,另取17.6g该样品,进行如下实验:

①实验时,先(填“加热样品”或“通一段时间的H2”)。
②通入足量H2加热,充分反应后,C中白色固体变蓝色,且增加1.8g。实验中D装置的作用是。
通过计算,得出样品中Cu2O质量为g,可知(填“乙”或“丙”)猜想成立。
体重 | 小于等于15kg | 5-23kg | 23-40kg | 大于40kg |
每次用量 | 30mg | 45mg | 60mg | 75mg |
假如患病儿童的体重是20kg,在治疗过程中,需每天服用“利托那韦”药片2次,一个疗程5天,那么该患儿一个疗程共服用粒。(每粒药片含“利托那韦”75mg)