 战汉时期老青铜错金马
B .
战汉时期老青铜错金马
B .  春秋战国青铜鎏金活链圆壶
C .
春秋战国青铜鎏金活链圆壶
C .  两周时期曾国编钟
D .
两周时期曾国编钟
D .  潮汕陶瓷工夫茶具
潮汕陶瓷工夫茶具
 C . Mn2+的价电子的轨道表示式:
C . Mn2+的价电子的轨道表示式:| 物质性质 | 物质用途 | |
| A | Na2O2吸收CO2产生O2 | Na2O2用作呼吸面具供氧剂 |
| B | Al2O3熔融状态可电离 | 电解熔融Al2O3制取单质Al |
| C | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| D | HF与SiO2反应 | HF在玻璃器皿上刻蚀标记 |
| 家务劳动 | 化学知识 | |
| A | 用白醋除去水壶中的水垢 | 白醋可溶解CaCO3沉淀 |
| B | 用小苏打粉作膨松剂焙制糕点 | NaHCO3加热容易分解放出CO2 |
| CD | 用含NaClO的84消毒液拖地 | NaClO有还原性 |
| 用洁厕灵洗马桶 | 洁厕灵中含有盐酸,可以与尿垢反应 |
| 叙述Ⅰ | 叙述Ⅱ | |
| A | NH3能使酚酞溶液变红 | NH3可用于设计喷泉实验 |
| B | 1-己醇的沸点比己烷的沸点高 | 1-己醇和己烷可通过蒸馏初步分离 |
| C | Al2O3熔点高,硬度大 | 实验室可用氧化铝坩埚熔化NaOH固体 |
| D | Na在Cl2中燃烧生成离子晶体 | NaCl固体可导电 |

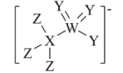
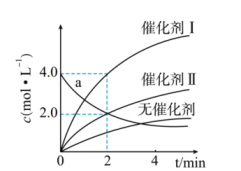
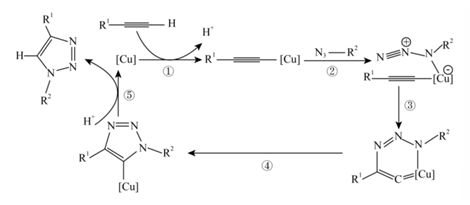
下列说法正确的是( )
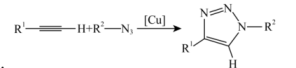 D . 一价铜[Cu催化剂能有效降低总反应的焓变
D . 一价铜[Cu催化剂能有效降低总反应的焓变
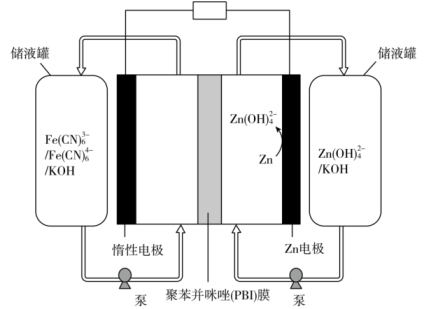
下列说法错误的是( )


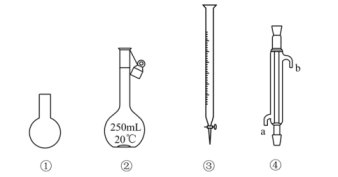
仪器a的名称是。
实验数据如表所示:
|
实验编号 |
电压/V |
pH |
阳极现象 |
阴极现象 |
|
1 |
1.5 |
5.52 |
无气泡,滴加KSCN显红色 |
无气泡,银白色金属析出 |
|
2 |
3.0 |
5.52 |
少量气泡,滴加KSCN显红色 |
无气泡,银白色金属析出 |
|
3 |
4.5 |
5.52 |
大量气泡,滴加KSCN显红色 |
较多气泡,极少量金属析出 |
|
4 |
1.5 |
1.00 |
无气泡,滴加KSCN显红色 |
较多气泡,极少量金属析出 |
①由实验1、2现象可以得出结论:增大电压,优先于放电;
②若由实验1、4现象可以得出结论:。
|
实验编号 |
c(NH4Cl)/mol·L-1 |
温度/℃ |
待测物理量 |
实验目的 |
|
5 |
0.5 |
30 |
a |
-- |
|
6 |
1.5 |
i |
b |
探究浓度对氯化铵水解平衡的影响 |
|
7 |
0.5 |
35 |
c |
ii |
|
8 |
2.0 |
40 |
d |
探究温度、浓度同时对氯化铵水解平衡的影响 |
该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol·L-1硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量”是;
②实验目的ii是;
③上述表格中,bd (填“>”、“<”或“=”)。
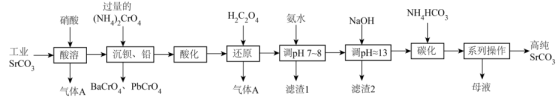
已知:①Sr(OH)2 为强碱,Cr(OH)3 为两性氢氧化物;
②常温下,各物质的溶度积常数如表所示。
|
化合物 |
Cr(OH)3 |
Ca(OH)2 |
Mg(OH)2 |
SrCO3 |
|
Ksp近似值 |
1×10-31 |
5.5×10-6 |
1.8×10-11 |
5.6×10-10 |
回答下列问题:

CO2(g)+H2(g) CO(g)+H2O(g) △H2 =b kJ·mol-1
2CO(g)+O2(g) 2CO2(g) △H3=c kJ·mol-1
则催重整反应CO2(g)+CH4(g) 2CO(g)+2H2(g)的△H=kJ·mol-1

①判断该反应的△H0 (填“>”、“<"或“=”),比较压强的大小: p1 p2 (填“>”、“<”或“=”)
②在恒容容器中进行该催化重整反应(不考虑其他反应),下列能说明该反应处于化学平衡状态的是 (填字母)。
A.CO2的质量分数保持不变.
B.容器中CO与H2的百分含量之比保持不变
C.v正(CH4)= 2v逆(CO)
D.容器中混合气体的平均相对分子质量保持不变
③X点对应的初始投料比n(CH4)/n(CO2)=1,平衡压强为P4,温度为950℃,则X点平衡常数Kp=


电解过程中阳极电极反应式为。
(i)分子中含有苯环;(ii) 能与NaHCO3溶液反应放出气体;(iii)分子中只有4种不同化学环境的氢原子。
 的合成路线(其它试剂任选,可不注明反应条件)。
的合成路线(其它试剂任选,可不注明反应条件)。