

已知: K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定,难溶于醇等有机溶剂。下列说法错误的是:( )


 制取氨气
B .
制取氨气
B .  提纯Cl2(含少量HCl、H2O)
C .
提纯Cl2(含少量HCl、H2O)
C .  制备Fe(OH)2
D .
制备Fe(OH)2
D . 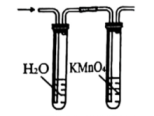 验证溴乙烷发生消去反应后产物的性质
验证溴乙烷发生消去反应后产物的性质


已知:①水溶液中铟主要以In3+的形式存在。
②In3++3HXInX3+3H+
回答下列问题:

In3+(aq)+3H2O(I) In(OH)3(aq)+3H+(aq),则该反应的化学平衡常数
K=(计算结果保留两位有效数字,常温下Kap[ In(OH)3]=1.3×10-37)。
Ⅰ.NH4ReO4的纯度测定
称取w g NH4ReO4样品,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1mLc1mol·L-1的盐酸标准溶液吸收,蒸氨结束后取下接收瓶。取吸收液用c2mol·L-1NaOH标准溶液滴定过剩的HCl, 达到终点时消耗V2mLNaOH溶液。

部分指示剂变色的pH范围如下表:
| 指示剂名称 | 变色的pH范围 | 酸色. | 中性色 | 碱色 |
| 甲基橙 | 3.1--4.4 | 红 | 橙 | 黄 |
| 甲基红 | 4.4一6. 2 | 红 | 橙 | 黄 |
| 溴百里酚蓝 | 6.0-7.6 | 黄 | 绿 | 蓝 |
| 酚酞 | 8.2-10.0 | 无 | 浅红 | 红 |
高温下用H2还原NH4ReO4可制得金属铼,装置如下图所示:
[已知:NH4ReO4 受热分解生成Re2O7]
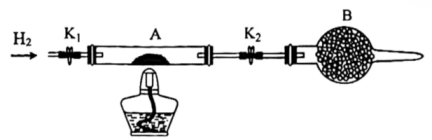
② 装置B中盛放的试剂为(填名称)。
②判断A中NH4ReO4已经反应完全的方法是。
③玻璃管内发生反应的化学方程式为。

△H=+123kJ·mol-1
已知:上述反应的速率方程为v正=k正P乙苯 , v逆=k逆P苯乙烯P氯气 , 其中k正、k逆分别为正、逆反应速率常数、P为各组分分压(分压=总压×物质的最分数)。
| 键 | C-H | C-C | C=C | H-H |
| 键能/kJ·mol-1 | 413 | 348 | X | 436 |
请计算X=kJ·mol-1。
 )脱氢的反应机理如下。
)脱氢的反应机理如下。 
下列说法正确的是 。

①图中n(乙苯):n(H2O)=1 :9的曲线是( 填曲线标号)。
②图中M点的正反应速率和N点的逆反应速率大小关系为v( M)正v(N)逆(填“>”“<”或“=”)。
③550℃、100 kPa,按n(乙苯):n(H2O)=1:9投料时,=kPa (用最简分数表示)。
a.离子键
b.c金属键
c.配位键
d.极性共价键

①甘氨酸铜中铜原子的杂化类型为(填“sp”或“dsp?” )。
②已知顺式甘氨酸铜能溶于水,反式甘氨酸铜难溶于水的原因可能是。

一个晶胞中有个O。已知1号O原子分数坐标为(0, 0,),2号O原子分数坐标为(
,
-m,
-n),则3号Fe原子的分数坐标为。
①苯环上有2个取代基
②与NaHCO3溶液反应产生气体
③遇FeCl3溶液发生显色反应
上述同分异构体中,核磁共振氢谱显示五组峰的结构简式为。