 B . 读取液体体积
B . 读取液体体积 C . 点燃酒精灯
C . 点燃酒精灯  D . 闻气体气味
D . 闻气体气味
选项 | 现象或事实 | 微观解释 |
A | 品红在热水中的扩散速度比在冷水中更快 | 受热时分子能量增大,运动速率加快 |
B | 6000 L氧气在加压情况下可装入容积为40 L的钢瓶中 | 加压时气体分子间隔变小 |
C | 金刚石无色透明,石墨深灰色不透明 | 原子种类不同 |
D | 氧气能供给呼吸,臭氧不能供给呼吸 | 分子构成不同 |




选项 | 实验目的 | 实验方法 |
A | 鉴别一氧化碳和甲烷 | 点燃,将生成的气体通入澄清石灰水中 |
B | 比较酒精灯火焰各层温度 | 将一根火柴梗迅速平放入火焰,约1 s后取出 |
C | 探究水的组成 | 电解水并检验所得产物 |
D | 验证质量守恒定律 | 在烧杯中称量铁与硫酸铜溶液反应前后物质总质量 |


途径①中的燃料属于(填“可"或“不可”)再生能源,燃料中的一些杂质如硫等燃烧时,还可能带来的另一个环境问题是。
元素名称 | 元素总量/t | 元素名称 | 元素总量/t | 元素名称 | 元素总量/t |
氧 | 3.35×1015 | 钾 | 0.1×1013 | 铜 | 1.1×107 |
氢 | 0.4×1015 | 溴 | 2.5×1011 | 镍 | 0.8×107 |
氯 | 7.2×1013 | 氟 | 0.5×1010 | 铝 | 0.8×107 |
钠 | 4.0×1013 | 磷 | 2.7×108 | 锰 | 0.8×107 |
镁 | 0.5×1013 | 碘 | 2.3×108 | 钛 | 0.4×107 |
硫 | 0.3×1013 | 铁 | 0.4×108 | 银 | 1.4×105 |
钙 | 0.2×1013 | 锡 | 1.1×107 | 金 | 0.15×104 |
海水中含量最多的金属离子是(填离子符号)。


【提出问题】熔喷布由哪些元素组成?
【查阅资料】
①无水硫酸铜为白色粉末,能吸收水分,遇水变蓝;
②熔喷布易燃,只可能由C、H、O中的两种或两种以上元素组成。
【提出猜想】

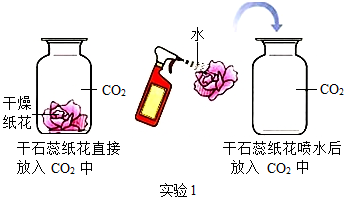
实验一:直接点燃熔喷布(如图1)
甲组同学采用直接点燃熔喷布的方法进行实验,用干冷烧杯、内壁涂澄清石灰水的烧杯分别罩在火焰上方,观察到的现象,得出:“熔喷布中一定含有碳元素和氢元素”。
实验步骤:
步骤1:连接装置,检查装置的气密性;
步骤2:将m克某熔喷布样品碎片装入玻璃管中,先通入一段时间干燥的氧气,再点燃酒精灯;
步骤3:一段时间后,待样品完全燃烧,无灰分残留;
步骤4:熄灭酒精灯,再持续通一会儿干燥氧气;
步骤5:冷却,称量,装置C增重m1克,装置D增m2克(所加药品均足量)。
“步骤4”中再持续通一会儿干燥氧气的目的是。
现象与结论:
得出结论:猜想①正确。
经过讨论:大家一致认为在装置C、D之间连接一个如图3所示的装置E会更严谨,理由是,可能发生反应的化学方程式为。