 B . 冰川融化
B . 冰川融化 C . 燃放烟花
C . 燃放烟花 D . 葡萄酿酒
D . 葡萄酿酒




加入物质 | 酚酞试液 | Na2CO3溶液 | FeCl3溶液 |
现象 | 变红 | 白色沉淀 | 红褐色沉淀 |
选项 | 物质 | 杂质(少量) | 除杂方法 |
A | N2 | O2 | 通过灼热的碳粉 |
B | NaCl固体 | 泥沙 | 溶解、过滤、蒸发结晶 |
C | CaCl2溶液 | HCl | 加入过量碳酸钙,充分反应后过滤 |
D | NaCl 溶液 | MgCl2 | 加入过量的NaOH溶液,充分反应后过虑 |
①一种助燃性气体单质;
②一种可做干燥剂的金属氧化物;
③一种易分解的酸;
④一种难溶性的碱;
⑤一种难溶性的盐。
①水的天然循环给陆地带来淡水;在水中氢元素与氧元素的质量之比为 (填最简整数比)。液态水变成水蒸气的过程中,水分子运动速率 (填“增大”“减小”“不变”之一)。
②积极应对气候变化,二氧化碳是实现“碳达峰”和“碳中和”目标的指标性物质。山东“十四五”规划提出二氧化碳每年控制在1134万吨,若二氧化碳年排放1100万吨,则其中含碳元素的质量为万吨(结果精确至0.1万吨)。
③生活垃圾实现分类回收,既可以保护环境又能节约资源、能源。生活垃圾分为可回收物、有害垃圾、厨余垃圾和其他垃圾四类。下列各项中,属于有害垃圾的是(填选项序号之一)。

A.废纸旧报 B.废旧灯管 C.瓜皮果核 D.废旧钢材
④开发和利用新能源,有利于生态环境保护。氢氧燃料电池已得到广泛应用,在这种电池中,氢气和氧气通过化学反应生成水。下列有关说法中,不合理的是(填选项序号之一)。

A.氢气和氧气发生了化合反应 B.该电池反应生成的水不污染环境
C.该电池的使用过程中化学能转化为电能 D.当前用电解水的方法制备所需氢气成本很低



①t1℃时,NaCl的溶解度Na2CO3的溶解度 (填“大于”“等于”“小于”之一)
②在t1℃时,将15gNa2CO3固体加入到50g水中,用玻璃棒充分搅拌后,所得溶液中溶质与溶液的质量之比为(填最简整数比)。
③若Na2CO3中混有少量NaCl,想要提纯Na2CO3晶体,宜采用的方法是(填“蒸发结晶”“降温结晶”之一)。
④t1℃时,将相同质量的Na2CO3饱和溶液和NaCl饱和溶液均升温至t2℃,此时,Na2CO3溶液的溶质质量分数(填“大于”“等于”“小于”之一)NaCl溶液的溶质质量分数。

①所选仪器的连接顺序为(从左到右填写仪器序号字母)。
②上述生成氧气的化学方程式为。
③下列有关氧气性质的叙述中,错误的是(填下列选项序号之一)。
A.氧气具有可燃性 B.氧气具有氧化性
C.氧气能支持燃烧 D.氧气化学性质比较活泼
①所选装置的连接顺序为(从左到右填写装置序号字母)。
②制取二氧化碳所发生反应的化学方程式为。
①仪器B1的作用为;C处玻璃管内的现象。
②若反应进行完全后,称得仪器C中剩余物质的总质量为9.6g,则样品中氧化铁的质量为g(精确到0.1g)。
③若通过测量B2装置反应前后质量的变化,求样品中氧化铁的质量,其结果要比实际值(填“偏大”“偏小”“基本一致”之一)。
④对于该实验方案设计还存在不完善之处,你的具体改进方案是。

试根据实验过程和图示提供的信息进行分析推理,填写以下空白:
①气体C的化学式为,X的现象是:。
②请写出上述过程③中发生的一个化学反应方程式。
③溶液H中一定存在的金属阳离子是(填离子符号)。
④混合溶液B中确定存在的物质是(填化学式)。
⑤固体混合物A中不能确定是否存在的物质是,原因是:。
①开发 (举一例)等新能源,不仅可以部分解决化石能源紧缺问题,还可以减少对环境的污染。
②煤燃烧时加入石灰石成生石灰作为固硫剂制成型煤,可以减少 (填化学式)。气体和氮的氧化物等有害气体的排放,有效减少酸雨的形成。
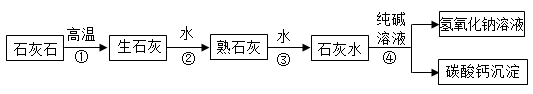
上述流程中,步骤①所涉及的反应类型为反应(填“化合”、“分解”,“置换”、“复分解”)写出上述转化流程步骤④中所发生反应的化学方程式。
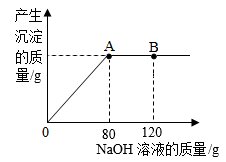
①当加入NaOH溶液120g时(即图中B点),烧杯中溶液里大量存在的阳离子是(填离子符号)。
②当加入NaOH溶液80g时(即图中A点),恰好完全反应试通过计算求产生沉淀质量。(计算结果精确至0.1g)