①Fe+2HCl=FeCl2+H2↑
②FeCl2+2NaOH=Fe(OH)2↓+2NaCl
③4Fe(OH)2+O2+2H2O=4Fe(OH)3
④2Fe(OH)3Fe2O3+3H2O
其中属于化合反应的是( )
 C .
C .  D .
D . 

 B .
B .  C .
C .  D .
D . 

①自来水生产中通入氯气的作用是。
②家用净水机中利用活性炭的性,除去水中有异味的气体。

①用如图所示装置收集一瓶纯净的氧气,通入气体前应将水加至(选填“甲”、“乙”、“丙”或“丁”)所示的高度,氧气应从管通入(选填“a”或“b”)。
②铁粉和水蒸气可制备磁性材料X,原理为3Fe+4H2OX+4H2 , X的化学式为。

①点燃氢气前必须。
②写出装有生石灰的干燥管中发生反应的化学方程式。
③若实验中观察到装有无水硫酸铜的干燥管中有蓝色固体,集气瓶壁上有水滴。该实验能否证明水是由氢元素和氧元素组成的? 理由是。
①写出仪器的名称:a,b。
②对装置甲检验气密性时,先用弹簧夹夹紧橡胶管,再向仪器a中加入适量水,观察到现象,说明气密性良好。
③将提供的试剂加入甲装置,发现生成气体太快,请写出一条改进方法。

①U型导管中不使用水的理由是。
②一段时间后,若c处液面高度(选填“高于”、“低于”或“等于”)d处液面高度,则证明二氧化碳能导致温室效应。
③使用绿色能源能减少二氧化碳的排放,请例举一种绿色能源。

温度(℃) | 20 | 90 |
NaCl的溶解度(g/100g水) | 36 | 39 |
①步骤1中分子的发生了变化。
A.间距 B.质量 C.种类 D.个数
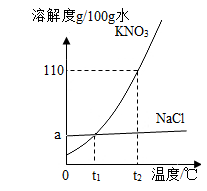
②属于饱和溶液的是(填溶液的编号)。
③溶液a中溶质的质量为g。溶液a经减压蒸发后得到溶液b和NaCl固体x g,x的数值为。溶液b的质量(选填“<”、“=”或“>”)溶液c的质量。
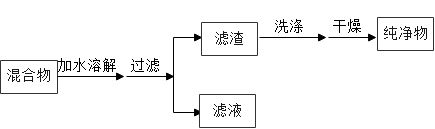
④分离溶液c和氯化钠固体的操作是。
⑤对比分析海水晒盐和真空制盐两种生产方法,各举一条优点。
优点 | |
海水晒盐 | |
真空制盐 |

实验一:装置见下图(省略夹持装置)。

①试管口略微向下倾斜的目的是。
②点燃酒精灯a,写出试管中发生反应的化学方程式,二氧化锰的作用是。
③待澄清石灰水中的导管口出现均匀连续的气泡,点燃酒精灯b。一段时间后,澄清石灰水变浑浊,写出该反应的化学方程式。该实验现象证明黑色固体中含。
实验二:在5支试管中分别混合对应的试剂,记录实验现象。
试管编号 | 试剂组合 | 实验现象 |
1 | 稀硫酸+木炭 | 无明显现象 |
2 | 稀硫酸+铜 | 无明显现象 |
3 | 稀硫酸+氧化铜 | 无色溶液变为蓝色 |
4 | 稀硫酸+木炭+铜 | 无明显现象 |
5 | 稀硫酸+混有黑色固体的红色金属 | 无色溶液变为蓝色 |
①稀硫酸中溶质的化学式为。
②根据实验现象,证明猜想正确。
红磷 | 木炭 | |
着火点(℃) | 260 | 约370 |

①实验1和实验3中的红磷燃烧,写出红磷燃烧的化学方程式。
②实验2中的木炭不燃烧的原因是。
③实验4中的红磷不燃烧的原因是。

①接通电源后,两电极上产生气泡,(选填“a”或“b”)管中的红磷先露出水面。
②通电一段时间,待两试管中液面都降至红磷下方后,停止通电,共消耗水0.036g,它的物质的量为mol,生成氧气摩尔。(根据化学方程式计算)。
③若试管内两块红磷的质量均为0.5g,用激光笔依次照射它们一段时间,观察到实验现象为。