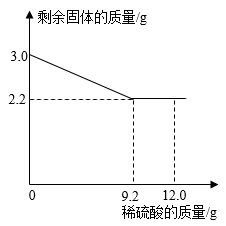
| 选项 | 实验目的 | 实验方案 |
| A | 除去MnO2中少量的KMnO4 | 加热固体混合物 |
| B | 除去CO2中少量的CO | 通入氧气后点燃 |
| C | 鉴别NaOH和NH4NO3两种固体 | 分别溶于等量水中,根据形成溶液的过程中温度的变化鉴别 |
| D | 鉴别KCl、(NH4)2SO4和尿素三种固体 | 分别加熟石灰研磨,根据能否嗅到氨味鉴别 |
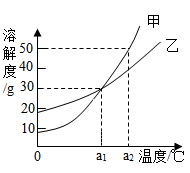
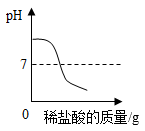 向一定质量的氢氧化钠溶液中逐滴加入稀盐酸
B .
向一定质量的氢氧化钠溶液中逐滴加入稀盐酸
B . 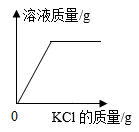 一定温度下,向接近饱和的氯化钾溶液中加入氯化钾固体
C .
一定温度下,向接近饱和的氯化钾溶液中加入氯化钾固体
C .  在密闭容器中用足量红磷燃烧测定空气中氧气的含量
D .
在密闭容器中用足量红磷燃烧测定空气中氧气的含量
D . 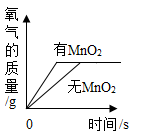 探究分解过氧化氢制氧气的反应中二氧化锰的作用
探究分解过氧化氢制氧气的反应中二氧化锰的作用
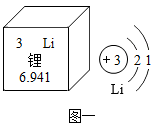
①锂元素的相对原子质量为,锂元素在化合物中通常显价。动力电池领域对氢氧化锂的需求量越来越大,请写出氢氧化锂的化学式。
②图二是铍元素的原子结构示意图,锂和铍在元素周期表中位于同周期的依据是。同周期金属元素的原子,随着核电荷数依次增多,失电子能力逐渐减弱,活泼性逐渐减小。由此可以推知:锂的活泼性(选填“大于”或“小于”)铍的活泼性。
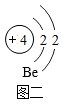
①锅里的油着火了,可采用的灭火措施是。
②区分陈醋和酱油,除品尝外,还可选用厨房中的(写俗称)来鉴别;
③患胃酸过多症的人常服用含氢氧化铝的药物来治疗,请用化学方程式表示其所依据的原理。
①铝的化学性质很活泼,通常铝制品却很耐腐蚀,原因是(用化学方程式表示)。
②将一定质量的锌粒投入到含有CuSO4和FeSO4的混合溶液中,充分反应后过滤,若滤液中只含有一种溶质,则滤渣中一定含有。
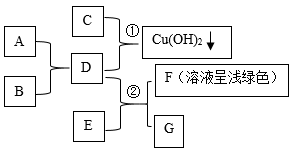
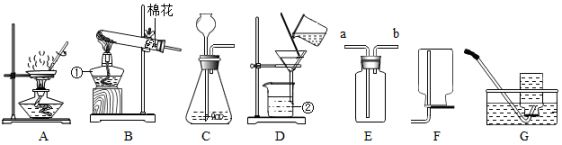
①对固液残留物进行过滤,应选择图中装置。
②取上述少量滤液进行蒸发,蒸发过程中玻璃棒不断搅拌的目的是,析出的固体中一定含有的物质是。
![]()
【提出问题】这瓶溶液是什么物质的溶液
【猜想与假设】老师提示:原溶液只可能是下列三种溶液中的一种:
猜想①氢氧化钠溶液 猜想②碳酸钠溶液 猜想③硫酸钠溶液
【查阅资料】Na2SO4溶液和BaCl2溶液均呈中性
同学 | 实验操作 | 实验现象及结论 | 同学相互评价 |
甲 |
| 溶液变红 猜想①成立 | 乙同学认为此方案结论不正确,你认为他的理由是。 |
乙 |
| 产生气泡 猜想②成立 | 丙同学认为:猜想①的溶液久置可能变质,加足量盐酸也会产生气泡 |
丙同学重新设计实验如下:
实验操作 | 实验现象 | 实验结论 |
步骤一:取少量样品溶液于试管中,加入过量BaCl2溶液,振荡 | 猜想①正确,且已部分变质。步骤二完毕后,溶液中除指示剂外。还含有的溶质有种(填数字)。 | |
步骤二:静置,取少量上层清液于另一支试管中,滴加 | 溶液变红 |
大家认为该实验方案仍然存在缺陷,如果氢氧化钠溶液已完全变质,则无法得出正确结论。
【实验反思】
①氢氧化钠变质的化学方程式为:,因此为了防止氢氧化钠变质,该试剂一定要密封保存。
②倾倒液体试剂,要注意标签朝向手心。
已知:CuO+H2SO4═CuSO4+H2O