 称取氢氧化钠
B .
称取氢氧化钠
B . 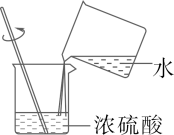 稀释浓硫酸
C .
稀释浓硫酸
C . 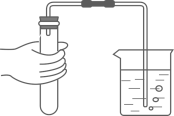 检查气密性
D .
检查气密性
D . 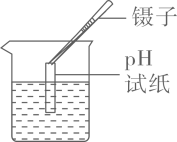 测定pH
测定pH
选项 | 物质(括号内为杂质) | 加入的除杂试剂及方法 |
A | CO2(H2) | O2、点燃 |
B | CaO(CuO) | 加水溶解、过滤 |
C | 稀硫酸(盐酸) | 加适量AgNO3溶液、过滤 |
D | Na2CO3(CaCO3) | 加水溶解、过滤、蒸发 |

选项 | 所用试剂 | 现象和结论 |
A | 硫酸铜溶液 | 出现蓝色沉淀,则氢氧化钠过量 |
B | 氯化钡溶液 | 出现白色沉淀,则硫酸过量 |
C | 锌粒 | 有气泡产生,则硫酸过量 |
D | 无色酚酞溶液 | 溶液不变色,则恰好完全反应 |
⑴取该固体粉末少量,加足量水,搅拌,静置,得到白色沉淀,上层为无色溶液;
⑵过滤,在白色沉淀中加入足量稀硝酸,白色沉淀有一部分溶解,且有无色气体产生.依据上述实验对原固体粉末的判断正确的是( )

K Ca Na Mg Zn Sn Pb ( ) Hg Pt Au

①铜比铁、铝更早被人类利用,主要原因是。
②欲比较铁、铜、银三种金属的活动性顺序,可选用的试剂是铁、、银。
③酸雨多发地区钢铁易受腐蚀,这是因为酸雨中含有的极少量硫酸会与铁发生反应,反应的化学方程式是。
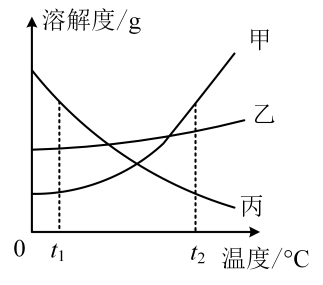
①t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是;
②t2℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数最大的是;
③t1℃时,甲和乙的饱和溶液升温到 t2 ℃时是;(填不饱和溶液或饱和溶液)。
④甲中混有少量乙,可用的方法除去。
|
温度/℃ |
0 |
10 |
20 |
30 |
40 |
|
|
溶解度/g |
KCl |
27.6 |
31.0 |
34.0 |
37.0 |
40.0 |
|
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
|
①请在图中补充另一种物质的溶解度曲线并标明两条曲线对应物质的名称;

②用氯化钠和蒸馏水配制 100 g 质量分数为 8%的氯化钠溶液。配制过程有以下步骤:a.称量及量取 b.计算 c.溶解 d.装瓶贴标签,正确顺序是;该实验中需要称量氯化钠g。
所需仪器:烧杯、量筒、胶头滴管和(填仪器名称)。

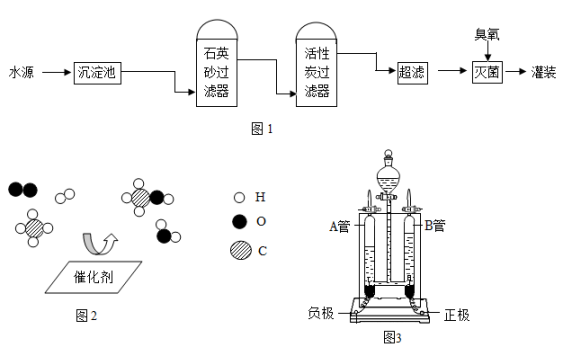
①收集二氧化碳通常选择的装置是(填序号)。
②小丽发现收集到的二氧化碳有刺激性气味,于是将气体从(填“a”或“b”)端通入装置 F 除去 HCl,再收集。
③用装置 A 做氯酸钾和二氧化锰制取氧气的实验,则装置 A 还需补充的仪器是, 请写出该反应的化学方程式:。
④组装仪器时连接玻璃管和胶皮管的操作:先把玻璃管口,然后稍稍用力即可把玻璃管插入胶皮管。
⑤若装置 G 中试管中的无色液体是水,向试管中加入一种固体,且 U 型管中 a 端液面下降、b 端液面上升,则所加固体可能是(填下列序号)。
A.冰 B.氧化钙 C.氢氧化钠 D.硝酸铵 E.干冰
⑥制取二氧化碳发生反应的化学方程式为,B 装置内碳酸钙的质量随时间变化的大致趋势如图所示,请结合图像分析,t0min 时 B 装置内的溶液中 Ca2+与 Cl-的个数比(填“等于” 或“小于”)1∶2。


步骤Ⅰ、向生石灰中加水制成石灰乳,将其温度降至室温;
步骤Ⅱ、将硫酸铜溶液慢慢倒入石灰乳中,边倒入边用木棒搅拌,即配成波尔多液。
①写出上述配制波尔多液过程中步骤Ⅰ和Ⅱ发生反应的化学方程式:Ⅰ、Ⅱ。
②阅读是学习的重要方式,在阅读信息中可以寻找答案,请根据题意找出步骤Ⅰ中石灰乳温度未降至室温,会造成波尔多液变质的原因。