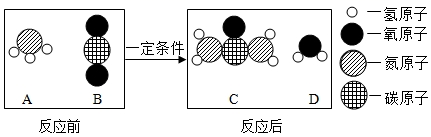
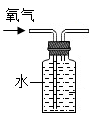
 收集一瓶氧气
B .
收集一瓶氧气
B . 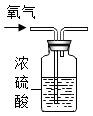 干燥氧气
C .
干燥氧气
C . 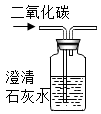 检验二氧化碳
D .
检验二氧化碳
D . 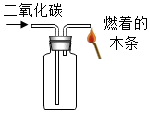 验满二氧化碳
验满二氧化碳
|
实验小组 |
第一组 |
第二组 |
第三组 |
第四组 |
|
水的质量(g) |
80 |
80 |
80 |
80 |
|
所取NaCl的质量(g) |
25 |
30 |
35 |
40 |
|
剩余NaCl的质量(g) |
0 |
2 |
7 |
12 |
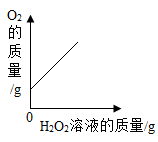 B . 镁在氧气中燃烧
B . 镁在氧气中燃烧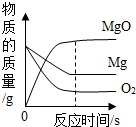 C . 等质量的锌、铁分别与质量分数相等且足量的稀硫酸反应
C . 等质量的锌、铁分别与质量分数相等且足量的稀硫酸反应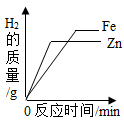 D . 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液
D . 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液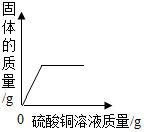
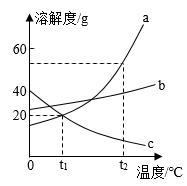

I.集气瓶中还有少量水 II.集气瓶口有大气泡冒出
若用上述药品制取二氧化碳
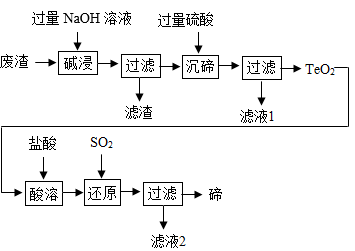
已知:TeO2微溶于水,易溶于较浓的强酸和强碱。
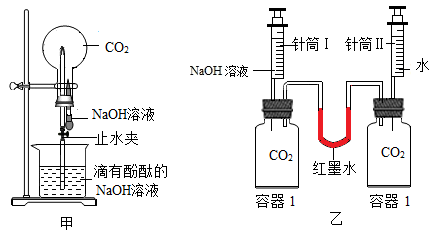
①利用图甲装置进行实验,先挤压胶头滴管,再打开止水夹,观察到烧瓶内形成红色“喷泉”,原因是烧瓶内压强(填“大于”或“小于”)外界大气压;
②利用图乙装置进行实验,分别将等体积的NaOH溶液和水同时注入盛有等体积CO2的玻璃容器中。证明CO2与NaOH溶液发生反应的实验现象是;
③写出CO2与NaOH溶液反应的化学方程式:。
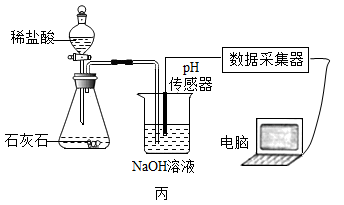
①写出图丙中制取CO2的化学方程式:,检验CO2的方法是;
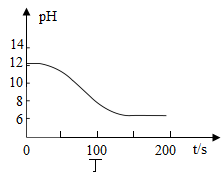
②实验测得烧杯中溶液的pH随时间的变化关系如图丁所示,可推知反应过程中浓度不断减小的离子是(填离子符号)。
①检验烧碱样品中是否含有Na2CO3 , 可选择的试剂是(填字母);
a.稀盐酸b.澄清石灰水c.酚酞
②计算烧碱样品中Na2CO3的质量分数(写出计算过程)。
【资料查阅】上述四种物质的相关信息如表:
|
物质 |
NaCl |
NaOH |
Na2CO3 |
NaHCO3 |
|
常温下的溶解度/g |
36 |
109 |
21.5 |
9.6 |
|
常温下稀溶液的pH |
7 |
13 |
11 |
9 |
请回答下列问题:
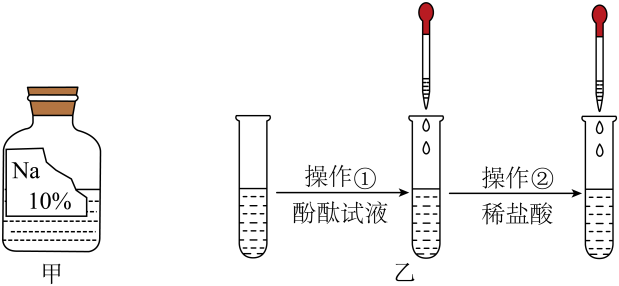
如图乙所示,在进行操作①时,酚酞试液变红色,由此可确定溶质不是(填化学式)。在操作②时,观察到的实验现象是,可确定溶质也不是NaOH。
【实验探究2】向操作①后试管中的溶液滴加过量CaCl2溶液(中性),充分反应后,试管中溶液颜色不变,但有白色沉淀产生。
【得出结论】通过实验探究2可确定原瓶溶液中的溶质应该是。
Ⅰ、现取样品16g于烧杯中并加84g水搅拌,全部溶解。再向烧杯中逐渐滴加26.1%硝酸钡溶液并不断搅拌,烧杯内固体的质量随加入硝酸钡溶液的质量的变化如图甲所示;
Ⅱ、在B点开始,向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图乙所示。
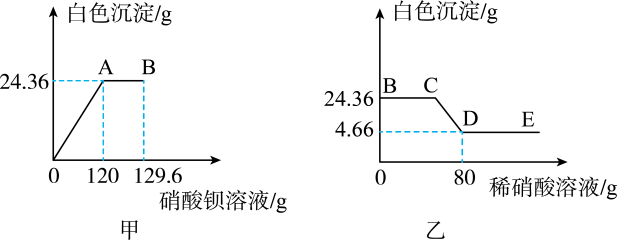
请回答下列问题: