 1,3-苯二酚
D .
1,3-苯二酚
D .  2-羟基丙烷
2-羟基丙烷
|
|
|
|
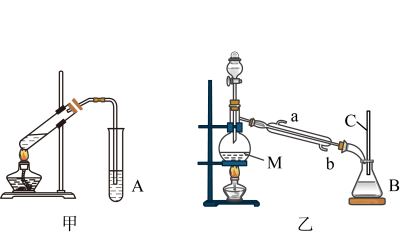
A.制备并收集乙酸乙酯 | B.除去甲烷中的乙烯 | C.验证溴乙烷的消去产物是乙烯 | D.分离乙醇和乙酸 |

① ②
②![]() ③
③![]() ④
④![]()
①蚁酸 ②乙醛 ③福尔马林 ④乙酸乙酯
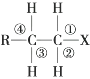

 B . 由丙烯合成聚丙烯的反应类型为加聚反应
C . 聚丙烯不能使酸性高锰酸钾溶液褪色
D . 聚丙烯在自然环境中容易降解
B . 由丙烯合成聚丙烯的反应类型为加聚反应
C . 聚丙烯不能使酸性高锰酸钾溶液褪色
D . 聚丙烯在自然环境中容易降解
① ②
② ③CH3OH④
③CH3OH④ ⑤
⑤ ⑥
⑥


![]()

①[Cr(H2O)4Cl2]Cl•2H2O中Cr3+的配位数为。
②硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是,在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为。
③氨是分子(填“极性”或“非极性”),中心原子的轨道杂化类型为,氨的沸点高于PH3 , 原因是。
